Analisi qualitativa organica
L’analisi qualitativa organica è notevolmente diversa dall’analisi qualitativa delle sostanze inorganiche. L’analisi qualitativa organica si avvale infatti di una serie di saggi specifici per individuare il gruppo funzionale presente in una molecola
Nonostante i composti organici siano numerosissimi, generalmente essi possono essere raggruppati in un numero piuttosto limitato di serie omologhe.
L’individuazione della serie a cui il composto appartiene rende più semplice il riconoscimento del composto stesso. In genere la prima operazione che si compie nell’analisi qualitativa organica per il riconoscimento di un composto organico è la determinazione delle costanti chimico-fisiche: il punto di fusione dei composti solidi, il punto di ebollizione dei composti liquidi. Segue l’analisi qualitativa degli elementi accertandosi se, oltre al carbonio e all’idrogeno, siano presenti altri elementi come l’azoto, lo zolfo, gli alogeni ecc. La presenza o l’assenza di tali elementi permette quindi di escludere immediatamente intere classi di composti organici e di rendere più limitato il campo di indagine.
Principali test nell’analisi qualitativa organica
Ricerca del carbonio e dell’idrogeno
Se è necessario provare o confermare la presenza di tali elementi si mescola una piccola quantità di sostanza secca con ossido di rame in una provetta e si arroventa. Il carbonio si ossida così a biossido di carbonio che si riconosce per la sua proprietà di intorbidire una soluzione di idrossido di bario. L’idrogeno a sua volta si riconosce arroventando la sostanza con solfito di sodio con formazione di solfuro di idrogeno riconoscibile dal suo odore caratteristico.
Ricerca di altri elementi
Per riconoscere azoto, zolfo e alogeni si ricorre al metodo di Laissagne sviluppato dal chimico francese Jean Louis Lassaigne, che consiste nel fondere il composto in esame con sodio metallico.
Nella reazione l’azoto si trasforma in cianuro, lo zolfo si trasforma in solfuro, gli alogeni si trasformano nei corrispondenti alogenuri di sodio. Gli anioni così formati possono essere riconosciuti tramite analisi qualitativa inorganica. La presenza dell’ossigeno non si accerta tramite reazioni dirette, ma è dedotta dall’analisi quantitativa calcolandone la percentuale per differenza, dopo la determinazione di tutti gli altri elementi presenti nella sostanza. Per ricercare il fosforo si può ossidare la sostanza con acido nitrico fumante al fine di ottenere acido fosforico che può essere riconosciuto con la reazione del molibdato.
Solubilità
Esame della solubilità del composto. Viene eseguita tramite alcuni solventi quali acqua, etere etilico, soluzione acquosa di idrossido di sodio al 5%, acido cloridrico al 5%, acido solforico concentrato. In base alla solubilità in questi solventi e agli elementi presenti nel composto in esame, si può quindi far rientrare il composto stesso in gruppi di solubilità
Gruppi di solubilità
Gruppo I. Sostanze solubili in acqua e etere dietilico: i primi termini delle serie omologhe di alcoli, aldeidi, chetoni, acidi carbossilici, fenoli, esteri, anidridi, ammine, nitrili, polidrossifenoli
Gruppo II. Sostanze solubili in acqua ma non in etere: ossiacidi e acidi poliossidrilici, glicoli, alcoli poliossidrilici, poliidrossi-aldeidi e chetoni (zuccheri), alcune ammidi, acidi solfonici e solfinici, sali amminoacidi, amminoalcoli, composti poliamminici
Gruppo III. Sostanze solubili in NaOH 5%: acidi, fenoli, immidi, ossime, tioli e tiofenoli, acidi solfonici, solfinici, solforici, solfonammidi, alcuni dichetoni e β- chetoesteri
Gruppo IV. Sostanze solubili in HCl 5%: ammine primarie, ammine secondarie alifatiche , ammine terziarie, idrazine
Gruppo V. Sostanze che non contengono azoto e zolfo solubili solo in acido solforico concentrato: idrocarburi insaturi, alcuni idrocarburi aromatici polialchilati, alcoli, aldeidi, chetoni, esteri, anidridi, acetali, lattoni, alogenuri acilici
Gruppo VI. Sostanze che non contengono azoto e zolfo insolubili in acido solforico concentrato: idrocarburi saturi alifatici, idrocarburi paraffinici ciclici, idrocarburi aromatici e loro alogeno-derivati, eteri diarilici
Gruppo VII. Sostanze contenenti azoto o zolfo, sostanze non incluse nei gruppi : I, II, III e IV: nitroso composti terziari, ammidi e derivati di aldeidi e di chetoni, nitrili, alcune ammine sostituite, nitroso, azocomposti e idrazocomposti, solfoni, alcune solfonammidi, solfuri e solfati
Classi di composti organici e loro reazioni caratteristiche
Per l’analisi qualitativa si suddividono i composti per classi e si valutano quindi le loro reazioni
Idrocarburi saturi
1) Saggio con una soluzione diluita di bromo in tetracloruro di carbonio: si forma acido bromidrico, i cui vapori si riconoscono mediante una cartina indicatrice
2) Saggio con una soluzione acquosa di permanganato di potassio al 5%: si ha decolorazione del reattivo
Alogeno-derivati
Saggio con una soluzione alcolica di nitrato di argento: precipita l’alogenuro di argento
Aldeidi e chetoni
Saggio con 2,4-dinitrofenilidrazina: sia aldeidi che chetoni danno luogo a fenilidrazoni poco solubili. In caso di saggio positivo la presenza di aldeidi viene effettuata con reazioni caratteristiche delle aldeidi
Aldeidi
1) Saggio con il reattivo di Schiff: questo reattivo è costituito da una soluzione di cloridrato di fucsina decolorata con biossido di zolfo: le aldeidi producono una colorazione rosa. I chetoni non reagiscono
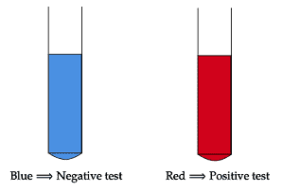
2) Saggio con il reattivo di Fehling: questo reattivo è costituito da una soluzione di solfato di rame che viene aggiunto a una soluzione alcalina di tartrato sodico-potassico. Le aldeidi producono una colorazione rossa perché reagiscono con il rame (II) riducendolo a rame (I) . I chetoni invece non reagiscono
3) Saggio con il reattivo di Tollens: il reattivo è costituito da una soluzione di nitrato di argento in idrossido di ammonio. Le aldeidi reagiscono formando uno specchio metallico sulle pareti del recipiente causata dalla riduzione dell’argento (I) ad argento metallico. I chetoni non reagiscono
Esteri e anidridi
1) Saggio con idrossilammina: sia gli esteri che le anidridi reagiscono formando acidi idrossammici, i quali reagiscono a loro volta con cloruro di ferro (III) formando sali complessi caratteristici, generalmente di colore violetto; i lattoni che sono esteri interni reagiscono analogamente
2) Saponificazione con alcali: da un estere si forma un alcol e il sale dell’acido; da un estere fenolico si formano i sali dell’acido e del fenolo; da un’anidride, invece, si forma il sale dell’acido corrispondente; si distilla la soluzione alcalina e nel distillato si può riconoscere l’alcool mentre nel residuo della distillazione si può riconoscere l’acido
Alcoli
1) Saggio con sodio: si svolge idrogeno
2) Saggio con cloruro di acetile: gli alcoli primari e secondari formano esteri; gli alcoli terziari formano prevalentemente il cloruro alchilico
Esteri
1) Saggio con sodio: nessuna reazione
2) Saggio con cloruro di acetile: nessuna reazione
3) Saggio con acido iodidrico: si ha idrolisi con formazione dei corrispondenti ioduro
Acidi carbossilici
1) Saggio con una soluzione di NaHCO3 al 5%: si ha dissoluzione e svolgimento di CO2
2) Titolazione con idrossido di sodio al 5%: si determina il peso equivalente dell’acido titolando con una soluzione di NaOH 0.1 N, in ambiente acquoso o alcolico usando come indicatore la fenolftaleina
Fenoli
1) Saggio con una soluzione di NaHCO3 al 5%: generalmente i fenoli non si sciolgono
2) Titolazione con idrossido di sodio al 5%: si ha dissoluzione. Dalla soluzione così ottenuta i fenoli sono riprecipitati mediante biossido di carbonio
3) Saggio con bromo: per reazione del bromo in tetracloruro di carbonio, i fenoli liberano acido bromidrico
4) Saggio con cloruro di ferro (III): in soluzione acquosa o alcolica si formano composti caratteristici variamente colorati (blu, rossi, verdi) di formula generale [Fe(OAr)6]3-
5) Saggio con anidride ftalica in acido solforico: si formano ftaleine caratteristiche
Ammine
1) Saggio con cloruro di acetile o con anidride acetica: le ammine primarie e secondarie danno luogo ad ammidi sostituite. Le ammine terziarie non reagiscono
2) Saggio con cloruro di benzoile: le ammine primarie e secondarie danno luogo a benzoilderivati, insolubili in soluzione alcalina
3) Reazioni con acido nitroso: le ammine aromatiche primarie danno luogo a sali di diazonio, che possono copulare con i fenoli formando coloranti azoici, di colori caratteristici. Le ammine aromatiche secondarie, invece, formano nitroso-derivati, che danno luogo alla reazione di Liebermann. Tale reazione consiste nel trattare la nitrosammina con fenolo in acido solforico a caldo. Si libera quindi acido nitroso che, reagendo con il fenolo, forma indofenolo il cui colore rosso diventa blu in soluzione alcalina. Le ammine aromatiche terziarie, invece, formano p-nitroso-derivati, che non danno la reazione di Liebermann
Nitrosoderivati
1) Riduzione in soluzione acida: per trattamento con stagno e acido cloridrico, i nitroderivati danno luogo ad ammine; per reazione con zinco in soluzione di cloruro di ammonio si ottengono idrossilammine, che si riconoscono per la loro azione riducente su una soluzione ammoniacale di nitrato d’argento
2) Reazione con cloruro di titanio (III): riduzione ad ammine
Ammidi
1) Idrolisi in soluzione alcalina: le ammidi primarie reagiscono con idrossido di sodio liberando ammoniaca
2) Idrolisi in soluzione acida: le ammidi sostituite, che resistono all’idrolisi in soluzione alcalina, si idrolizzano in acido solforico dando luogo ai corrispondenti acidi ed ammine
Nitrili
1) Idrolisi in soluzione alcalina: per riscaldamento con una soluzione di idrossido di sodio si ottiene il sale dell’acido
2) Idrolisi in soluzione acida: con acido solforico concentrato si ottiene un’ammide
Le determinazioni delle costanti fisiche, l’esame della solubilità e la ricerca dei gruppi funzionali permettono di riconoscere la classe a cui appartiene il composto. Per l’identificazione del composto stesso si ricerca, in apposite tabelle quel composto che presenta costanti molto vicine al composto analizzato. Il composto in esame è a questo punto fatto reagire al fine di ottenere un composto di sostituzione di cui si determinano le costanti fisiche. Pertanto se queste coincidono con quelle di un derivato di uno dei composti presi in considerazione, si può dedurre che quest’ultimo composto e il composto in esame sono identici



