Norbornene
Il Biciclo[2.2.1]ept-2-ene noto come norbornene appartiene alla famiglia dei composti biciclici che ha formula C7H10. Il norbornene è un alchene ciclico con una struttura tridimensionale costituito da un anello di cicloesene con un metilene a ponte tra le posizioni 1 e 4 e un doppio legame in posizione 2.
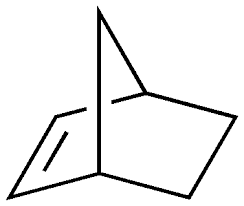
Il norbornene è solubile in etanolo e in molti solventi organici ed utilizzato come monomero nelle reazioni di polimerizzazione e quale intermedio nelle sintesi organiche. Allo stato naturale si presenta come un solido bianco con un odore caratteristico.
Il doppio legame di questa struttura biciclica produce una tensione dell’anello, che può essere rilasciata, trasformandolo in un alchene altamente reattivo ed in particolare con varie forme allotropiche dello zolfo come zolfo S8 e S10 e le specie contenenti zolfo come, ad esempio, i tioli. Inoltre, il norbornene e i relativi analoghi insieme all’adamantano, tricicloalcano con formula C10H16 , sono diventati le strutture policicliche più sfruttate come specie non aromatiche e non planari nella progettazione di nuovi farmaci.
Sintesi del norbornene
Il norbornene può essere sintetizzato, con una resa di circa il 74% dalla reazione tra l’1,3-ciclopentadiene e etene condotta alla temperatura di 200°C e alla pressione di 200 atm. La reazione di sintesi è tipicamente una reazione di Diels-Alder che prende il nome dai chimici tedeschi Otto Diels e Kurt Alder che la scoprirono nel 1928 e vinsero il premio Nobel per la Chimica nel 1950.

La reazione Diels-Alder è una reazione organica di tipo stereospecifico che viene utilizzata per convertire un diene coniugato e un dienofilo che, nel caso del norbornene sono rispettivamente l’1,3-ciclopentadiene e l’etene. Il meccanismo della reazione di Diels-Alder procede attraverso l’interazione tra un sistema di 4 π elettroni con un sistema di 2π elettroni e prevede una cicloaddizione che portano alla formazione di un nuovo anello da due reagenti.
Nella reazione Diels-Alder, il sistema di elettroni 4 π si riferisce alla struttura dienica mentre il sistema di elettroni 2 π si riferisce alla struttura dienofila e, poiché i legami π vengono convertiti in legami σ più forti, la reazione è termodinamicamente favorita. L’intera reazione avviene in un’unica fase in presenza di calore secondo un meccanismo concertato in cui i legami si formano e si rompono allo stesso tempo.
Reazioni
A causa della presenza del doppio legame dà le reazioni tipiche degli alcheni come, ad esempio, l’idrogenazione catalitica a seguito della quale si ottiene il norbornano ovvero il biciclo[2.2.1]eptano, idrocarburo saturo biciclico a testa di ponte avente formula molecolare C7H12.
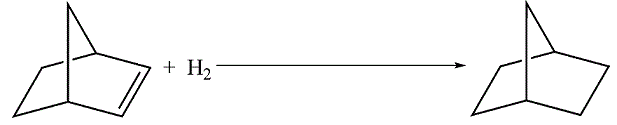
Un’altra reazione è quella di idratazione in cui si fa reagire il norbornene in acqua in presenza di un catalizzatore acido, tipicamente l’acido solforico per dare un alcol detto norbornano.
Poiché quando l’acido solforico si trova a contatto con l’acqua si verifica una reazione esotermica onde evitare che la temperatura si innalzi troppo il recipiente di reazione viene immerso in un bagno di acqua e ghiaccio. Nel primo stadio della reazione (lento) elettrofilo H+ si somma al carbonio con ibridazione sp2 per dar luogo alla formazione di un carbocatione intermedio planare.

Nel secondo stadio della reazione (veloce) avviene la reazione del carbocatione con il doppietto elettronico solitario presente sull’ossigeno della molecola di acqua che si comporta da base di Lewis. L’ossigeno legatosi al carbocatione, caricato positivamente, espelle un idrogeno sotto forma di ione H+ con relativa formazione di un alcol. Dei due potenziali diastereomeri che si possono formare ovvero l’endo-norborneolo con il gruppo -OH in posizione pseudo assiale e l’eso-norborneolo con il gruppo -OH in posizione pseudo equatoriale si forma preferenzialmente l’eso-norborneolo.
La particolare reattività del norbornene, unita alle proprietà biologiche che questa molecola conferisce ad altre molecole, ha attirato l’attenzione dei ricercatori negli ultimi decenni, soprattutto nel campo della chimica farmaceutica e della ricerca sul cancro.
A causa della rapida reattività del norbornene e dei suoi derivati con diversi sostituenti attorno al suo scaffold nella formazione di polimeri che possono essere utilizzati come trasportatori di agenti chemioterapici o in applicazioni teranostiche questi composti sono stati studiati fin dal 1994
Polimeri
Il norborene costituisce il monomero nella polimerizzazione per metatesi ad apertura di anello delle olefine che dà, come prodotto di reazione, il polinorborene utilizzato nell’industria della gomma dove è richiesta una elevata resistenza alle vibrazioni o agli urti.
La polimerizzazione per metatesi ad apertura di anello è detta ROMP acronimo di Ring-opening metathesis polymerization, termine coniato dal chimico statunitense Robert Howard Grubbs vincitore del Premio Nobel per la Chimica nel 2005.
Catalizzatori Ziegler-Natta, catalizzatori metallocenici, catalizzatori non metallocenici a base di metalli di transizione che vanno dal gruppo 3 al gruppo 5 ovvero dallo scandio al vanadio e catalizzatori di metalli di transizione che vanno dal gruppo 9 al gruppo 11 ovvero dal cobalto al rame sono stati utilizzati per catalizzare la polimerizzazione del norbornene. Tuttavia, la catena polimerica non polare del polimero presenta diverse problematiche come la scarsa solubilità, fragilità meccanica e bassa compatibilità.

A seconda delle condizioni di reazione e del catalizzatore utilizzato, generalmente un metallo di transizione come molibdeno, rutenio, tungsteno, palladio e nichel tali monomeri possono essere polimerizzati secondo diversi meccanismi ovvero polimerizzazione cationica/radicalica e polimerizzazione per addizione di tipo vinilico, fornendo polimeri con diverse strutture delle catene principali.
La polimerizzazione coordinata del norbornene attraverso il suo doppio legame olefinico è un eccellente approccio catalitico poiché fornisce prodotti polimeri saturi, che presentano proprietà interessanti e uniche come elevata trasparenza, eccellente stabilità termica, elevata resistenza chimica e buona resistenza ai raggi UV. Il monomero inoltre può essere utilizzato per formare copolimeri con lo stirene, con l’acrilato di metile e con l’etene sebbene pochi catalizzatori abbiano raggiunto una copolimerizzazione efficiente.
Per ottenere ulteriori miglioramenti nelle proprietà, sono stati sviluppati copolimeri olefinici ciclici (COC) attraverso la copolimerizzazione coordinata di norbornene con vari alcheni in cui il doppio legame si trova in posizione 1 e come etene, propene, α –olefine superiori e anche monomeri polari.
I catalizzatori al nichel contenenti leganti sono stati ampiamente utilizzati nella copolimerizzazione del norbornene grazie al loro processo di iniziazione flessibile, elevata attività, buona stabilità e basso costo. Tali catalizzatori costituiscono quindi una buona base di partenza per ottenere copolimeri olefinici ciclici funzionalizzati.



