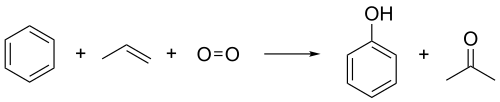Propene: sintesi, reazioni
Il propene è un idrocarburo insaturo che si presenta gassoso a temperatura ambiente che fa parte degli alcheni e ha formula CH2=CH-CH3
Dopo l’etene è il più semplice degli alcheni. Nella molecola in cui vi è un doppio legame carbonio-carbonio sono quindi presenti due atomi di carbonio ibridati sp2 e un atomo di carbonio ibridato sp3 .
Il propene si presenta come un gas incolore con un odore simile a quello del petrolio ed è utilizzato, come monomero di partenza per la sintesi del polipropilene.
Sintesi del propene
Questo gas è stato ottenuto per molti anni tramite due processi:
- Steam cracking che consiste nella pirolisi degli idrocarburi sotto forma di gas naturale in presenza di vapore acqueo
- Cracking catalitico
Tuttavia in entrambi i processi si ottengono altri prodotti di reazione pertanto, stante l’elevata richiesta di questo composto, la ricerca si è indirizzata a realizzare metodi in cui il prodotto principale della reazione fosse propene.
CH3CH2CH3 → CH2=CH-CH3 + H2
- Processo MTO (Methanol To Olefine) scoperto nel 1977 e utilizzato per convertire il metanolo in olefine. Il metanolo viene dapprima trasformato in dimetiletere:
2 CH3OH(g) → CH3OCH3(g) + H2O(g)
La miscela di gas viene fatta passare su un letto di zeolite che trasforma selettivamente l’etere in propene
CH2=CH2 + C4H8 → 2 CH2=CH-CH3
- Reazione tra etanolo e monossido di carbonio in presenza di idrogeno per ottenere 1-propanolo usando un catalizzatore costituito da un complesso di rutenio e cobalto:
CH3CH2OH + CO + 2 H2 → CH3CH2CH2OH + H2O
Dalla disidratazione dell’1-propanolo si ottiene il propene
Reazioni
Il propene dà le reazioni tipiche degli alcheni tra cui idrogenazione catalitica da cui si ottiene il propano, alogenazione da cui si ottiene un dialogenuro vicinale, addizione di acidi alogenidrici e idratazione.
Si tenga conto che le ultime due reazioni avvengono secondo un meccanismo che prevede la formazione di un carbocatione e, essendo il propene un alchene asimmetrico, i prodotti di reazione seguono la regola di Markovnikov pertanto l’addizione di HBr porta al 2-bromopropano e l’idratazione porta al 2-propanolo.
Tra le reazioni più tipiche del propene vi è:
- Formazione di ossido di propilene
Nella reazione il propene è fatto reagire con cloro e acqua con ottenimento di una miscela di cloridrine isomere costituita da 1-cloro-2-propanolo e 2-cloro-1-propanolo:
CH2=CH-CH3 + Cl2 + H2O → CH3CHClCH2OH e/o CH3CHOHCH2Cl
La cloridrina ottenuta è fatta reagire con una base come ad esempio idrossido di sodio ottenendosi una reazione di epossidazione con formazione dell’ossido di propilene
Allo stesso prodotto di reazione si può pervenire facendo reagire il propene con perossido di idrogeno o il propene con un idroperossido
- Formazione di butanale
Tramite una reazione di idroformilazione si può ottenere il butanale facendo reagire il propene con monossido di carbonio e idrogeno in presenza di una sale solido di cobalto:
CH2=CH-CH3 + CO + H2 → CH3=CH2CH2CHO
Il propene è fatto reagire con benzene e ossigeno per dare fenolo e acetone secondo il processo al cumene
Il propene è il monomero di partenza per la sintesi del polipropilene. Tale polimero viene ottenuto in presenza di catalizzatori Ziegler-Natta che, grazie alla loro scoperta, il chimico tedesco Karl Waldemar Ziegler e l’ingegnere chimico italiano Giulio Natta vinsero nel 1963 il Premio Nobel per la Chimica per “le loro scoperte nel campo della chimica e della tecnologia dei polimeri”.