Ciclopentene- sintesi, reazioni, usi
Il ciclopentene è un alchene ciclico insaturo presentando un doppio legame e ha formula C5H8 e struttura

I cicloalcheni hanno formula generale CnH2n-2 e presentano due siti di insaturazione
È un liquido incolore meno denso dell’acqua su cui galleggia essendo insolubile in essa. la sua solubilità in acqua è infatti di 0.535 g/L
Nel ciclopentene vi sono tre atomi di carbonio ibridati sp3 per i quali l’angolo di legame dovrebbe essere di 109.5° e due atomi di carbonio ibridati sp2 per i quali l’angolo di legame dovrebbe essere di 120°. Poiché l’angolo interno di un pentagono regolare è di 108°il ciclopentene non ha la tensione di anello che mostrano gli omologhi inferiori come il ciclobutene,
In natura si trova nel Trichoderma harzianum fungo utilizzato anche come fungicida
Sintesi del ciclopentene
Una via sintetica prevede l’idrogenazione catalitica del ciclopentadiene
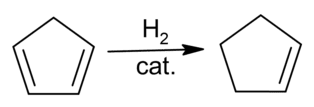
Può essere ottenuto
- per reazione del ciclopentano con etossido di sodio secondo la reazione:
C5H10 + CH3CH2ONa → C5H8 + CH3CH3 + NaOH - per disidratazione del ciclopentanolo
- per idrogenazione selettiva dell’1,2-3,4-ciclopentadiene
Reazioni
Esso può reagire in modo vigoroso con agenti ossidanti e può reagire secondo una reazione esotermica con agenti riducenti rilasciando idrogeno gassoso.
Dà luogo alle reazioni tipiche degli alcheni in presenza di:
- catalizzatori o di opportuni iniziatori dà luogo a reazioni di polimerizzazione.
- acqua, acetato di palladio e fosfato di molibdeno e vanadio il ciclopentene viene ossidato a ciclopentanone con rilascio di idrogeno gassoso.
- N-bromosuccinimmide e di un perossido organico dà luogo alla formazione di 3-bromociclopentene
- acqua e acido cloridrico dà luogo alla formazione del cloropentano
Usi
Viene utilizzato:
- per analizzare i meccanismi delle reazioni organiche
- come componente della benzina
- nelle reazioni di polimerizzazione
- per produrre gomma e plastica



