Tipi di amminoacidi
Vi sono diversi tipi di amminoacidi, alcuni dei quali indispensabili per l’organismo, che si trovano negli alimenti e svolgono determinate funzioni.
Tra i tipi di amminoacidi vi sono quelli:
- Essenziali
- A catena ramificata
- Non proteinogenici
- Chetogenici
- Glucogenici
Amminoacidi essenziali
Sono quei tipi di amminoacidi indispensabili che l’organismo non è in grado di sintetizzare ma vanno assunti con gli alimenti. Sono pertanto i più importanti tra i diversi tipi di amminoacidi
Le proteine sono polimeri i cui monomeri sono costituiti dai venti diversi tipi di amminoacidi presenti in natura. Gli amminoacidi sono composti che contengono nella loro molecola sia il gruppo carbossilico –COOH che il gruppo amminico –NH2 , basico.
Entrambi questi gruppi funzionali sono legati a un carbonio, chiamato carbonio-α. A questo carbonio, sono legati, inoltre, un atomo di idrogeno e un gruppo denominato genericamente R che, essendo diverso nei 20 tipi di amminoacidi, ci consente di differenziarli.
Nel processo digestivo le proteine si rompono per dare amminoacidi liberi nel tratto gastrointestinale. Essi sono assorbiti, passano in circolo e sono trasportati al fegato dove gruppi amminici sono rimossi dalla transaminazione. L’ alfa-cheto ottenuto è quindi utilizzato come fonte energetica o come intermedio biosintetico.
Funzioni
Gli amminoacidi, infatti, non sono immagazzinati nell’organismo come i grassi o i carboidrati ma, attraverso la sintesi proteica, vanno a costituire proteine che a seconda dei casi:
1) hanno una funzione strutturale in quanto concorrono a formare l’impalcatura del corpo; ad esempio il collagene è il principale componente fibroso delle ossa, dei tendini, della pelle, delle cartilagini, dei denti; i capelli e le unghie sono costituiti da α-cheratina;
2) svolgono funzione catalitica: gli enzimi, infatti, indispensabili catalizzatori biologici sono costituiti da proteine
3) fungono da mezzo di trasporto di altre molecole: nel sangue, ad esempio, l’ossigeno viene trasportato dall’emoglobina
4) provocano il movimento: ad esempio la contrazione muscolare è resa possibile da due proteine ovvero dall’actina e dalla miosina
5) hanno compiti protettivi: gli anticorpi, come le immunoglobuline che sono i più importanti mezzi di difesa dell’organismo sono costituiti da proteine
6) concorrono al sistema endocrino: vari ormoni, tra cui l’insulina sono costituiti da proteine
7) fungono da riserva di sostanze nutritive: ad esempio l’ovoalbumina del bianco dell’uovo e la caseina presente nel latte sono costituiti da proteine
8) rappresentano un sistema di controllo del pH del sangue perché limitano le eccessive variazioni di ioni H+ dovute al metabolismo cellulare.
Gli esseri umani non sono in grado di sintetizzare tutti e venti i tipi di amminoacidi necessari alla sintesi proteica: gli amminoacidi che non possono essere sintetizzati, ma devono essere necessariamente assunti tramite l’alimentazione sono detti amminoacidi essenziali.
Gli amminoacidi essenziali sono: fenilalanina, isoleucina, istidina, leucina, lisina, metionina, treonina, triptofano e valina.
Fenilalanina
È contenuta nella maggior parte delle proteine animali e vegetali, e partecipa alla formazione stessa di queste ultime. Inoltre è precursore di un altro amminoacido, la tirosina, che partecipa alla sintesi di ormoni tiroidei e molecole a funzione nervosa. Le principali fonti di fenilalanina sono tutti gli alimenti ricchi in proteine come carne, pesce e uova.
Isoleucina
Appartiene alla categoria degli amminoacidi ramificati ed è un amminoacido importante per la sintesi proteica, specialmente a livello muscolare. L’isoleucina, inoltre, è in grado di produrre glucosio o corpi chetonici in caso di digiuno o attività fisica prolungata oltre a partecipa alla produzione di emoglobina. Le principali fonti di isoleucina sono: bresaola, maiale, pollo, agnello, tonno, legumi, formaggio, uova e arachidi.
Istidina

È presente nell’emoglobina ed è il precursore dell’istamina che svolge un importante ruolo nei processi infiammatori. Inoltre l’istidina è un componente della carnosina antiossidante che si trova nei muscoli e nel cervello ed ha proprietà antiossidanti ed anti-invecchiamento. Le principali fonti di istidina sono: proteine della soia, legumi, merluzzo, carne, arachidi e biscotti per bambini.
Leucina
La leucina è importante per la crescita e aumenta la resistenza muscolare e, nei periodi di digiuno, fornisce energia al metabolismo. E’ uno dei tipi di amminoacidi molto utile nelle attività e in caso di sforzo fisico prolungato. La leucina è inoltre un carburante energetico importante nelle situazioni post-trauma, o in fase di infezione o stress. Le principali fonti di leucina sono: ricotta, sesamo, arachidi, lenticchie, pollo e pesce.
Lisina
Svolge numerose funzioni nel nostro organismo: oltre a essere presente insieme ad altri amminoacidi nella struttura del collagene, è uno dei precursori della niacina, vitamina la cui carenza può causare la pellagra.
La lisina favorisce la produzione di anticorpi, enzimi e ormoni e l’assorbimento di calcio.
Le principali fonti di lisina sono: carne suina, formaggi, germe di grano, latticini, lievito di birra, pesce.
Metionina
È il precursore di molte molecole quali la carnitina che ha la funzione di convertire gli acidi grassi in energia, la cisteina, la creatina, la taurina, la colina e la vitamina B12. Le principali fonti di metionina sono: latticini, carne bovina, albume, proteine della soia ed alcuni pesci come il merluzzo.
Treonina
Ha spiccate funzioni depurative per l’organismo in genere e alcuni organi specifici come fegato e reni. Tra le numerose funzioni della treonina importante è quella relativa alla rigenerazione dei tessuti in quanto ha una azione sulla elastina e collagene. Svolge una importante funzione nel sistema immunitario dato il suo ruolo nella formazione di anticorpi ed essendo un costituente degli stessi. Le principali fonti di treonina sono: biscotti, legumi, funghi, carni di maiale, agnello, coniglio e bovina, formaggi, uova e sardine.
Triptofano
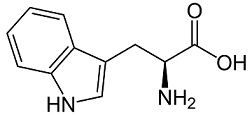
Interviene nella produzione della serotonina neurotrasmettitore presente soprattutto nel sistema nervoso centrale e nel tratto gastro-intestinale. Nell’apparato digerente, la serotonina regola la digestione, mentre a livello del sistema nervoso centrale, questo neurotrasmettitore è fondamentale per regolare l’umore, il sonno, l’appetito, l’apprendimento e la memoria. Il triptofano partecipa anche alla biosintesi di vitamine del gruppo B, specialmente niacina e vitamina B6 importanti in numerosissimi processi metabolici. Le principali fonti di triptofano sono: uova, latte e derivati, cane, salmone, cacao, cioccolato fondente, patate, banane, riso, cereali integrali, verdure a foglia verde, noci e mandorle.
Valina
Svolge importanti funzioni nella ricostruzione dei tessuti e in particolare in quelli muscolari. La valina è un amminoacido assorbito piuttosto velocemente dall’intestino ed è quindi disponibile abbastanza rapidamente per l’organismo dopo l’assunzione. Essendo un amminoacido ramificato può essere utilizzato specialmente dal muscolo come substrato energetico. Inoltre regola l’azione di molecole nervose. Le principali fonti di valina sono: latticini e prodotti caseari, carne di maiale e agnello, cereali, polvere della soia, uovo.
Amminoacidi a catena ramificata
Gli amminoacidi a catena ramificata sono leucina, isoleucina e valina: essi sono tutti amminoacidi essenziali ovvero devono essere necessariamente assunti con gli alimenti. Essi sono nutrienti essenziali che il corpo ottiene dalle proteine presenti negli alimenti, in particolare carne, latticini e legumi.
Gli amminoacidi a catena ramificata sono indicati con la sigla BCAA acronimo di Branched Chain Amino Acids. Hanno questa denominazione a causa della loro struttura che presenta una catena ramificata e rappresentano circa il 15-25% dell’apporto proteico totale.
Catabolismo
Tali amminoacidi, che sono i maggiori costituenti del tessuto muscolare, sono catabolizzati da enzimi che agiscono su tutti e tre.
Il primo stadio del catabolismo dei BCAA inizia con due stadi comuni catalizzati da enzimi che agiscono su tutti e tre gli amminoacidi:
1) transaminazione reversibile da aminotransferasi a catena ramificata;
2) decarbossilazione ossidativa irreversibile ad opera del complesso dell’α-chetoacido deidrogenasi a catena ramificata. A seguito di queste due reazioni si ottengono l’isovaleril-CoA dalla leucina, il 2-metilbutirril-CoA dall’isoleucina e l’isobutirril-CoA dalla valina.
Tutti e tre i prodotti delle reazioni subiscono una deidrogenazione catalizzata da tre diversi enzimi e a questo punto le loro vie divergono. La leucina viene convertita in acetil-CoA e acetoacetato, l’isoleucina in acetil-CoA e succinil-CoA e la valina in succinil-CoA. Nel muscolo tali prodotti possono essere completamente ossidati attraverso il ciclo di Krebs.
Integratori
Gli atleti utilizzano integratori a base di amminoacidi a catena ramificata per la loro capacità di stimolare la sintesi proteica.
Le caratteristiche e i benefici dei singoli amminoacidi a catena ramificata portano a un rapporto ottimale leucina, isoleucina e valina di 2:1:1.
Gli integratori possono essere assunti sia prima dell’allenamento in quanto aiutano a preservare il tessuto muscolare, forniscono energia e ritardano l’insorgenza dell’affaticamento mentre se assunti dopo l’allenamento migliorano il recupero e accelerano la rigenerazione del tessuto muscolare
Amminoacidi non proteinogenici
Gli amminoacidi non proteinogenici (NPAA) sono quei tipi di amminoacidi non codificati naturalmente nel codice genetico umano né si trovano nelle catene polipeptidiche.
Tuttavia, negli organismi come batteri, funghi, piante e animali marini sono elementi costitutivi essenziali delle catene polipeptidiche. Si differenziano dai tipi di amminoacidi proteinogenici che sono quelli usati per la costruzione delle proteine.
Numerosi amminoacidi non proteinogenici presenti in natura sono analoghi a quelli proteinogenici e alcuni esistono come metaboliti secondari in molti organismi.
Vi sono oltre 800 NPAA in natura e ne sono stati sintetizzati migliaia attraverso processi chimici e biocatalitici o tramite una combinazione di entrambi
Funzioni
Alcuni di questi metaboliti vegetali sono componenti del metabolismo centrale, fungendo da intermedi nelle vie biosintetiche o come molecole di segnalazione durante le risposte allo stress delle piante.
Gli NPAA come ornitina, citrullina, acido argininsuccinico, omoserina, omocisteina e cistationina sono intermedi metabolici ben studiati ed è probabile che siano presenti in tutte le specie vegetali.
Altri NPAA vegetali comunemente riscontrati, ad esempio l’acido pipecolico con i suoi derivati, possono funzionare come molecole di segnalazione che influenzano lo sviluppo delle piante, la fisiologia e le risposte di difesa.
Esempi di amminoacidi proteinogenici
Ornitina
Oltre che a partecipare al ciclo dell’urea è fondamentale per la produzione di proteine, enzimi e tessuto muscolare.
Inoltre è il punto di partenza per la sintesi di molte poliammine come putrescina e spermina e di vari altri importanti composti come l’acido glutammico e la prolina ed è necessaria per una corretta funzione immunitaria e una buona funzionalità epatica
Citrullina
La citrullina è un α-amminoacido non essenziale avente formula C6H13N3O3 che partecipa attivamente al ciclo dell’urea.
È una sostanza che potenziali ruoli antiossidanti e vasodilatatori. All’interno dell’organismo è in grado di reagire con l’acido aspartico per formare l’acido argininsuccinico, successivamente trasformato in arginina.
Acido argininsuccinico
Le cellule sintetizzano l’acido arginosuccinico dalla citrullina e acido aspartico e lo usano come precursore dell’arginina nel ciclo dell’urea
Omoserina
Differisce dalla serina in quanto presenta un gruppo -CH2 aggiuntivo.
È il precursore dell’arginina nel ciclo dell’urea ed è un intermedio nella biosintesi di tre amminoacidi essenziali metionina, treonina e isoleucina.
Omocisteina
È biosintetizzata dalla metionina mediante la rimozione del suo gruppo metilico terminale ed è un omologo della cisteina da cui differisce in quanto presenta un gruppo -CH2 aggiuntivo.
Quando interagisce con le vitamine del gruppo B, l’omocisteina si converte in:
- metionina amminoacido essenziale e antiossidante
- cisteina amminoacido non essenziale sintetizzato dalla metionina che riduce l’infiammazione, aumenta la comunicazione tra le cellule immunitarie e migliora la salute del fegato.
Amminoacidi chetogenici
Gli amminoacidi chetogenici (KAA) sono quei tipi di amminoacidi che possono essere degradati in acetil-CoA o acetoacetato e possono quindi portare alla produzione di acidi grassi o corpi chetonici .
I corpi chetonici sono composti idrosolubili ovvero acetone, acido acetoacetico e acido β-idrossibutirrico.
I corpi chetonici sono trasportati dal fegato ad altri tessuti, dove l’acetoacetato e il β-idrossibutirrato possono essere riconvertiti in acetil-CoA per produrre energia, tramite il ciclo di Krebs. Un accumulo di corpi chetonici è detto chetosi condizione in cui l’organismo ottiene energia bruciando i grassi e producendo chetoni.
Mentre la grande maggioranza dei corpi chetonici è sintetizzata dall’acetil CoA che deriva dalla β -ossidazione degli acidi grassi nei mitocondri, una piccola quantità può essere sintetizzata dagli amminoacidi chetogenici
Gli amminoacidi chetogenici si differenziano quindi dagli amminoacidi glucogenici in quanto questi ultimi possono essere impiegati per essere convertiti a glucosio tramite il processo di gluconeogenesi.
Gli amminoacidi che sono sia chetogenici e glucogenici sono triptofano, fenilalanina, tirosina, isoleucina e treonina mentre quelli rimanenti sono esclusivamente glucogenici
Lisina e leucina sono gli unici amminoacidi puramente chetogenici, poiché vengono degradati nei precursori per la sintesi del corpo chetonico, acetil-CoA e acetoacetato.
Lisina
Il primo passo nella via catabolica della lisina è la reazione con α-chetoglutarato con formazione della saccaropina.
Le reazioni coinvolte, catalizzate dalle saccaropine deidrogenasi, sono:
lisina + α-chetoglutarato ⇌ saccaropina ⇌ glutammato + 2-aminoadipato 6-semialdeide
Il catabolismo dell’acido 2-aminoadipico procede attraverso la decarbossilazione a una serie di esteri di CoA che terminano in acetil-CoA.
Leucina
Nella prima fase della degradazione della leucina avviene la transaminazione dall’amminoacido per produrre α-chetoisocaproato. Quest’ultimo è decarbossilato per formare isovaleril-CoA che, a seguito di deidrogenazione, forma il β-metilcrotonil-CoA .
Il β-metilcrotonil-CoA è carbossilato dall’enzima etilcrotonil-CoA carbossilasi per formare β-metilglutaconil-CoA che è quindi idratato dalla β-metilglutaconil-CoA idratasi per formare β-idrossi-β-metilglutaril-CoA.
Esso è poi scisso in acetil-CoA e acetoacetato. L’enzima che catalizza quest’ultimo stadio è la 3-idrossi-3-metilglutaril-CoA (HMG-CoA) liasi.
Amminoacidi glucogenici
Gli amminoacidi glucogenici GAA sono quei tipi di amminoacidi che possono essere impiegati per essere convertiti a glucosio tramite il processo di gluconeogenesi.
Si differenziano dagli amminoacidi chetogenici che sono convertiti in corpi chetonici.
Il metabolismo di alcuni amminoacidi può portare alla formazione di più di uno degli intermedi metabolici e questi amminoacidi appartengono a entrambe le categorie.
Il catabolismo degli amminoacidi glucogenici produce piruvato o uno degli intermedi nel ciclo di Krebs mentre quello degli amminoacidi chetogenici produce acetil CoA o acetoacetil CoA.
Lo scopo principale del catabolismo proteico durante uno stato di digiuno o sforzo prolungato è fornire gli amminoacidi glucogenici soprattutto alanina e glutammina. Essi, infatti, fungono da substrati per la produzione endogena di glucosio. Gli scheletri di carbonio sono convertiti in piruvato, 2-ossoglutarato, succinil-CoA, fumarato e ossalacetato e agiscono come precursori del glucosio.
Gluconeogenesi
La gluconeogenesi è un processo metabolico che avviene nel citosol e nei mitocondri necessario a mantenere costante il livello di glucosio nel sangue durante lo stato di digiuno o durante un intenso sforzo fisico
Essa avviene a partire da precursori non saccaridici come amminoacidi glucogenici, lattato, piruvato e glicerolo e ha luogo prevalentemente nel fegato ed in piccola parte nella corteccia surrenale.
Il glucosio prodotto tramite la gluconeogenesi è quindi rilasciato nel flusso sanguigno in modo che possa essere utilizzato per produrre energia.
Gli amminoacidi glucogenici sono:
Alanina
Arginina
Asparagina
Acido aspartico
Cisteina
Acido glutammico
Glutammina
Glicina
Istidina
Metionina
Prolina
Serina
Valina
Amminoacidi catabolizzati in piruvato
L’alanina è convertita in piruvato da una reazione catalizzata dall’enzima alanina aminotransferasi. Essa trasferisce in modo reversibile il gruppo amminico dall’ alanina al 2-ossoglutarato per produrre piruvato e glutammato. Successivamente, il 2-ossoglutarato è rigenerato dalla glutammato deidrogenasi, dal glutammato.
La serina è convertita in piruvato da una reazione catalizzata dalla serina deidratasi, che consente la β eliminazione del gruppo ossidrile per formare un intermedio amminoacrilato che a sua volta si tautomerizza nell’immina, che è poi idrolizzata per produrre piruvato.
La glicina è convertita in piruvato per conversione iniziale in serina mediante una reazione catalizzata dall’enzima serina idrossimetil transferasi.
La cisteina può essere convertita in piruvato attraverso diversi percorsi, ad esempio i tre atomi di carbonio della cisteina possono essere convertiti in cistationina che a sua volta si trasforma in piruvato e omocisteina
La treonina è un amminoacido che è sia glucogenico che chetogenico. La via di degradazione più comune riguarda la formazione di acetil-CoA e glicina. Quest’ultimo è successivamente convertito in serina dalla serina idrossimetiltransferasi e quindi la serina è trasformata in piruvato dalla serina deidratasi.
Amminoacidi catabolizzati ad ossalacetato
L’aspartato e l’ asparagina sono entrambi catabolizzati in ossalacetato.
L’aspartato è convertito in ossalacetato da una reazione catalizzata dall’enzima aspartato aminotransferasi, che trasferisce un gruppo amminico dall’aspartato al 2-ossoglutarato per produrre glutammato e ossalacetato.
L’asparagina è idrolizzata in aspartato e ammoniaca attraverso una reazione catalizzata dall’enzima asparaginasi .
Amminoacidi catabolizzati a 2-ossoglutarato
Glutammina, prolina , arginina e istidina sono prima convertite in glutammato e poi subiscono deaminazione per produrre 2-ossoglutarato.
Amminoacidi catabolizzati in succinil-CoA
La metionina, la valina e l’isoleucina sono catabolizzate in propoinil-CoA che è convertito in d -metilmalonil-CoA dalla propionil-CoA carbossilasi tramite la β-ossidazione degli acidi grassi. Il d -metilmalonil-CoA è successivamente racemizzato in l -metilmalonil-CoA dalla metilmalonil-CoA racemasi. La reazione catalizzata dalla metilmalonil mutasi alla fine produce succinil-CoA.
La degradazione della metionina richiede nove passaggi, uno dei quali prevede la sintesi di S -adenosilmetionina.
https://chimicamo.org/biochimica/amminoacidi-essenziali/
https://chimicamo.org/biochimica/amminoacidi-glucogenici/
https://chimicamo.org/biochimica/amminoacidi-a-catena-ramificata/
https://chimicamo.org/biochimica/amminoacidi-non-proteinogenici/



