Metiltriossorenio: proprietà, sintesi, epossidazione degli alcheni, usi
Il metiltriossorenio (MTO) noto nei paesi anglosassoni come methyltrioxorhenium(VII) è un composto organometallico in cui il renio ha numero di ossidazione +7. Ha formula CH3ReO3 e in esso il renio è legato a un gruppo metilico e a tre atomi di ossigeno tramite doppio legame. Pertanto secondo la teoria V.S.E.P.R. una geometria tetraedrica e struttura:
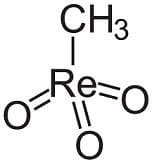
Proprietà del metiltriossorenio
È un solido cristallino, volatile, incolore, solubile in acqua e si comporta da acido di Lewis e come ossidante
È solubile in acetonitrile, benzene, cloroformio, etanolo, etere etilico e scarsamente in solfuro di carbonio e n-esano. Il metiltriossorenio è utilizzato quale catalizzatore insieme al perossido di idrogeno per l’ossidazione di una varietà di substrati.
Fu scoperto per la prima volta nel 1979 da Beattie e Jones mediante ossidazione all’aria del trimetiltriossorenio. Idrolizza rapidamente in soluzioni acquose basiche e molto più lentamente in mezzi acidi.
Sintesi
Può essere preparato attraverso diverse vie sintetiche a partire, ad esempio, dalla reazione dell’eptossido di renio e tetrametilstagno:
Re2O + (CH3)4Sn → CH3ReO3 + (CH3)3SnORnO3
Si può ottenere, per reazione di un sale dell’acido perrenico come il perreato di potassio con il tetrametilstagno
Il tetrametilstagno è un composto organometallico che si ottiene dalla reazione tra tetracloruro di stagno e lo ioduro di metilmagnesio che è un reattivo di Grignard
Epossidazione degli alcheni
Il metiltriossorenio è utilizzato quale ossidante catalitico per convertire gli alcheni in epossidi in una varietà di solventi. L’epossidazione degli alcheni è una delle reazioni più esplorate nella sintesi organica poiché gli epossidi sono importanti intermedi organici ampiamente utilizzati. Da essi, inoltre, si possono ottenere resine epossidiche per la realizzazione di materiali compositi avanzati. Inoltre, gli epossidi possono anche essere usati per ottenere detergenti e tensioattivi.
La reazione avviene in presenza di perossido di idrogeno, o una miscela di perossido di idrogeno, urea e percarbonato di sodio. Sebbene gli epossidi possano essere sintetizzati in modo non catalitico, su piccola scala mediante peracidi e su larga scala utilizzando il processo della cloridrina, tutti i nuovi sviluppi mirano a processi catalitici al fine di ridurre i sottoprodotti, i rifiuti e i costosi ossidanti.
Usi del triossido di metilrenio
È usato come catalizzatore eterogeneo in molte reazioni.
Supportato su allumina e silice, catalizza a 25°C la metatesi delle olefine che consiste nello scambio dei sostituenti presenti su olefine diverse. Questa reazione è usata in campo pertolchimico per ottenere propene da etene e 2-butene.
Il metiltriossorenio è usato come catalizzatore per la conversione di alchini terminali a acidi carbossilici mentre, se il triplo legame è contenuto all’interno della molecola, si ottengono dichetoni
Catalizza anche la conversione di:
- aldeidi e diazoalcani in alcheni
- 2-metilnaftalene in 2-metil-1,4-naftochinone
- ossidazione di ammine a N -ossidi con percarbonato di sodio



