Naftalene: struttura, proprietà, reazioni, usi
Il naftalene, noto anche come naftalina, è un idrocarburo biciclico aromatico costituito da due anelli benzenici fusi. Si trova negli oli essenziali di numerose specie vegetali quali, ad esempio, la magnolia. Ha formula C10H8 e struttura
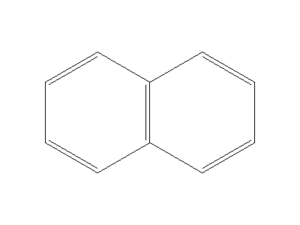
La struttura molecolare è quella di due anelli benzenici fusi insieme a due atomi di carbonio adiacenti comuni ad entrambi gli anelli. Quando sono presenti due o più sostituenti si devono numerare gli atomi di carbonio come indicato nella figura

Proprietà
E’ un solido cristallino di colore bianco caratterizzato da un odore pungente; ha un punto di fusione di 80°C, un punto di ebollizione di 218 °C ma presenta la caratteristica di sublimare ovvero di passare a temperatura ambiente dallo stato solido a quello di vapore. E’ insolubile in acqua, poco solubile in etanolo e solubile in benzene, etere, cloroformio e solfuro di carbonio.
Il naftalene, insieme ad altri idrocarburi policiclici aromatici, è originato sia da processi di combustione incompleta che avvengono sia nelle industrie che dal fumo di sigaretta e dal fumo di scarico di veicoli a motore nonché da eventi come gli incendi boschivi.
Nel suo comportamento chimico mostra il carattere aromatico del benzene e dei suoi derivati e dà luogo a reazioni di sostituzione elettrofila in cui un atomo di idrogeno viene sostituito da un alogeno, un nitrogruppo, un gruppo alchilico, un gruppo acilico, un gruppo solfonico.
Reazioni del naftalene
Tra le reazioni tipiche ricordiamo:
1) Sintesi del 2-naftolo
Il 2-naftolo è analogo al fenolo, sebbene più reattivo, ed è un solido incolore fluorescente ed è usato come intermedio per la produzione di coloranti.

Il 2-naftolo è ottenuto a partire dal naftalene in un processo a due stadi:
– solfonazione del naftalene in acido solforico:
C10H8 + H2SO4 → C10H7SO3H + H2O
– il naftalene solfonato viene poi trattato con idrossido di sodio fuso secondo la reazione:
C10H7SO3H + 3 NaOH → C10H7ONa + Na2SO3 + 2 H2O
La neutralizzazione del prodotto dà il 2-naftolo C10H7OH.
2) Sintesi dell’ 1-naftolo
L’1-naftolo è un isomero del 2-naftolo e viene sintetizzato a partire dal naftalene in un processo a più stadi:
– nitrazione del naftalene con ottenimento dell’1-nitronaftalene:
C10H8 + HNO3 → C10H7NO2 + H2O
– idrogenazione con ottenimento di un’ammina:
C10H7NO2 + 3 H2 → C10H7NH2 +2 H2O
– idrolisi dell’ammina con ottenimento dell’1-naftolo
C10H7NH2 + H2O → C10H7OH + NH3
3) Ossidazione del naftalene a anidride ftalica (Processo Gibbs-Wohl)
L’ossidazione del naftalene avviene in presenza di ossigeno ed è catalizzata dal ossido di vanadio (V):
4) Sintesi dell’1-naftilammina
La sintesi dell’1-naftilammina si ottiene per riduzione dell’1-nitronaftalene in presenza di ferro e HCl. La miscela di reazione è poi trattata con Ca(OH)2 per neutralizzare l’ambiente di reazione e successivamente si procede alla distillazione. E’ il precursore di derivati da cui si ottiene il Rosso Congo
Usi
Il naftalene è usato nella produzione di materie plastiche, coloranti, resine, lubrificanti e combustibili. Come pesticida il naftalene era usato per tarme e altri parassiti anche se è stata sostituita dal meno tossico p-diclorobenzene.
L’esposizione ad alte concentrazioni può danneggiare i globuli rossi del sangue fino a provocare anemia emolitica.
Il naftalene è nocivo e si ritiene possa avere effetti cancerogeni: lasciamo quindi a Eta Beta la sua alimentazione a base di palline di naftalina e maneggiamo con cura e circospezione tale sostanza evitandone quanto più il contatto.




