Elettrocromismo
L’elettrocromismo è un fenomeno associato alla variazione reversibile e persistente delle proprietà ottiche di alcune sostanze prodotto dall’applicazione di un campo elettrico che induce un flusso di elettroni e ioni all’interno del materiale e quindi a processi di ossidazione e riduzione. Il passaggio dallo stato ossidato a quello ridotto porta alla formazione del colore, cioè alla formazione di nuovi picchi spettrali nell’area visibile.
L’elettrocromismo è correlato ad alcuni materiali in grado di innescare reazioni redox reversibili sotto stimolazione elettrica esterna, modificando così in modo reversibile il loro colore e/o le loro proprietà ottiche come, ad esempio, assorbanza e trasmittanza. Queste proprietà sono state utilizzate in numerose aree come la progettazione di strutture avanzate, dispositivi medici impiantabili, dispositivi ottici e rivestimenti elettronici artificiali.
Gli ossidi dei metalli di transizione a base di tungsteno, vanadio, nichel, molibdeno, titanio, iridio e numerose sostanze organiche mostrano il fenomeno dell’elettrocromismo che, sebbene sia stato studiato a partire dagli ultimi venticinque anni del XX secolo, già nel 1815 Berzelius dimostrò che l’ossido di tungsteno puro di colore giallo pallido cambiava colore durante la riduzione quando riscaldato sotto un flusso idrogeno e nel 1824 Wöhler effettuò una riduzione chimica simile con sodio metallico.
Durante la prima metà degli anni ’70 si esplorato l’uso dell’elettrocromismo nei display e diverse grandi aziende come IBM, Philips e Canon hanno compiuto notevoli sforzi di ricerca. Tuttavia, l’elettrocromismo fu accantonato in quanto i display furono realizzati utilizzando i cristalli liquidi che presentano frequenze di aggiornamento elevate essendo in grado di passare più velocemente dallo stato trasparente a quello opaco, in frazioni di secondo.
Materiali elettrocromici
I materiali elettrocromici possono essere costituiti da composti inorganici come ioduro di rame (I) CuI, cromato di piombo e biossido di vanadio, piccole molecole organiche come Bis(dietilammonio) tetraclorocuprato (II) [(C2H5)2NH2 ]2CuCl4 , polimeri coniugati e polimeri a cristalli liquidi e derivati del triarilmetano.
Alcuni polimeri coniugati come polianilina e politiofene e polimeri a cristalli liquidi come poliesteri aromatici parzialmente cristallini basati su acido 4-idrossibenzoico, che possiedono proprietà termocromiche sono promettenti materiali che mostrano elettrocromismo.
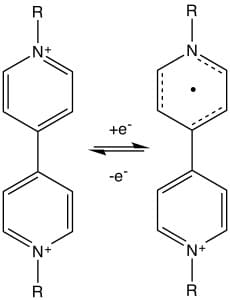
Altri materiali che mostrano elettrocromismo sono i viologeni, sali organici costituiti da uno ione alogenuro e dal catione γ, γ′-dipiridinio, derivato del dipiridile che hanno la proprietà di assumere, in seguito a riduzione, un’intensa colorazione. La molecola di viologeno ha due anelli di carbonio collegati, ciascuno con una sostituzione di azoto, e si colora di blu quando viene ridotta elettrochimicamente.
Rispetto agli ossidi dei metalli di transizione, i polimeri coniugati, macromolecole costituite da unità ripetitive in cui l’intera catena principale del polimero è legata insieme non solo da legami σ saturi, ma anche da legami π insaturi, hanno vantaggi quali commutazione redox inferiori, risposta più rapida, maggiore efficienza di colorazione e colori più diversificati.
Grazie al comportamento di commutazione ottica, i materiali elettrocromici offrono grandi opportunità per una varietà di applicazioni di risparmio energetico e regolazione del colore, tra cui finestre intelligenti, display bistabili multicolori ed elementi ottici con regolazione del colore.
I materiali elettrocromici vengono normalmente depositati come film sottili e possono assumere numerose architetture come un unico film elettrocromico, situato sull’anodo o sul catodo o una disposizione ha più pellicole elettrocromiche, posizionate sia sull’anodo che sul catodo, e colorate simultaneamente per un maggiore contrasto.
Elettrocromismo e finestre intelligenti
Nel 1984, è stato proposto di utilizzare la tecnologia dell’elettrocromismo negli edifici ad alta efficienza energetica e da allora la ricerca sui materiali elettrocromici ha avuto un potente impulso. Tale tecnologia è utilizzata nelle vetrate, negli specchietti per autoveicoli, negli specchietti retrovisori, nei tettucci apribili, negli occhiali da sole.
Il termine “finestra intelligente” è stato coniato nel alla fine del 1984 e ha attirato immediatamente l’attenzione non solo degli scienziati ma anche dei media e del pubblico in generale perché l’utilizzo di questa tecnologia permette di risparmiare energia negli edifici consentendo un risparmio dovuto all’utilizzo di minori quantità di energia per il condizionamento estivo, così come per il riscaldamento invernale di oltre il 30% rispetto alle finestre convenzionali.
Una finestra intelligente è una finestra a risparmio energetico che regola la radiazione solare combinando materiali oscuranti con vetro e altri substrati. Una finestra intelligente ideale, applicabile universalmente a tutti i tipi di edifici e alle zone climatiche, controlla in modo indipendente la trasmissione della luce solare visibile e del calore solare in un edificio.
Il fatto che il comportamento possa essere controllato dinamicamente consente a proprietari, gestori e utenti di adattare la facciata in vetro elettrocromico intelligente alle loro esigenze, che possono cambiare nel corso della giornata e, naturalmente, stagionalmente.
Per questo motivo, il controllo indipendente sulle regioni visibili e del vicino infrarosso dello spettro solare è un obiettivo chiave per i dispositivi elettrocromici avanzati potendo contribuire a un’efficienza energetica ottimale nei sistemi di riscaldamento, raffreddamento e illuminazione artificiale di un edificio. Il vetro intelligente in cui si manifesta l’elettrocromismo cambia la sua trasmittanza se stimolato da un segnale elettrico. Questo cambiamento reversibile altera lo stato del vetro tra trasparente e opaco.
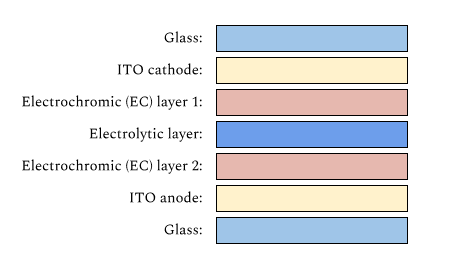
Un pannello di vetro che sfrutta l’elettrocromismo è composto da una pila di strati che ha normalmente uno spessore di pochi micron ed è creato utilizzando la stessa tecnica di deposizione fisica in fase di vapore (PVD) utilizzata nell’industria manifatturiera dei semiconduttori.
Sui pannelli di vetro esterni sono presenti strati conduttivi trasparenti, normalmente di ossido di indio-stagno (ITO), che convertono l’intera struttura in qualcosa di simile a una batteria, dove l’ITO comprende gli elettrodi. Al centro della struttura si trovano lo strato di accumulo ionico, lo strato conduttore ionico (elettrolitico) e lo strato elettrocromico (EC) che insieme sono responsabili della variazione della trasmittanza.
Quando si applica una tensione diretta alla struttura, le particelle cariche come gli ioni di litio migrano dallo strato di accumulo degli ioni, attraverso l’elettrolita, allo strato elettrocromico spesso l’ossido di tungsteno, che è trasparente nel suo stato inattivo.
Ciò fa sì che lo strato elettrocromico subisca una reazione di ossidoriduzione che comporta un assorbimento della luce e ciò ne provoca la colorazione. Quando si inverte la tensione, gli ioni di litio tornano indietro dallo strato elettrocromico, attraverso l’elettrolita, e di nuovo allo strato di accumulo degli ioni, riportando il vetro al suo stato trasparente. Questo cambiamento di stato può avvenire nell’ordine di minuti.
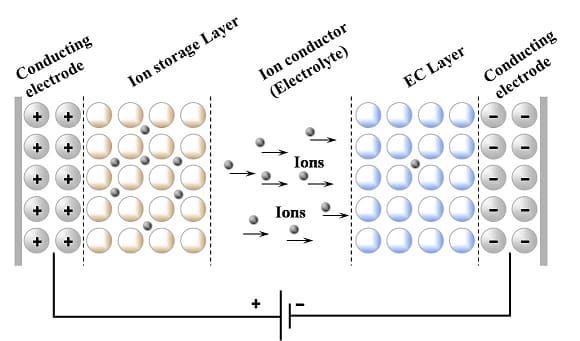
Quando viene applicata una tensione attraverso lo strato elettrocromico, gli ioni di litio si intercalano cioè si inseriscono nello strato elettrocromico riducendo il gap di banda dell’ossido di tungsteno a circa 2 eVolt, il che significa che i fotoni incidenti aventi almeno quell’energia possono essere assorbiti dall’ossido di tungsteno, energizzando gli elettroni in uno stato energetico più elevato.
Poiché i fotoni della luce visibile hanno almeno questa energia, vengono assorbiti dallo strato elettrocromico intercalato, e si può vedere che la radiazione solare che raggiunge l’occhio umano passando attraverso il vetro manca di quelle lunghezze d’onda, cioè manca di luce visibile e quindi appare colorato.
Dispositivi elettrocromici
I dispositivi elettrocromici possono funzionare in modalità assorbente o riflettente, dove entrambe le modalità hanno almeno un elettrodo otticamente trasparente. Modalità assorbente: gli esempi includono occhiali, visiere o vetri intelligenti dotati di un secondo elettrodo posteriore otticamente trasparente. Modalità riflettente: gli esempi includono display informativi e specchi antiriflesso che hanno un metallo lucido dietro l’elettrodo posteriore.
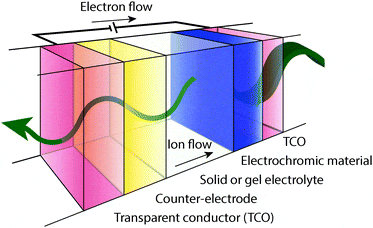
Un tipico rivestimento che sfrutta l’elettrocromismo per finestra è un dispositivo multistrato costituito da uno strato di elettrodo elettrocromico attivo, uno strato di controelettrodo, uno strato di elettrolita che separa i due elettrodi, due strati conduttori trasparenti che fungono da conduttori elettrici e substrati di supporto. I due strati degli elettrodi sono spesso costituiti da ossidi di metalli di transizione.
Quando il dispositivo è spento i cationi, come Li + o H + si trovano nell’elettrolita e nel controelettrodo mentre quando è acceso, una tensione applicata tra gli strati conduttori opposti spinge i cationi a migrare dal controelettrodo, attraverso l’elettrolita, nell’elettrodo elettrocromico, modificandone lo stato di ossidazione e le sue proprietà ottiche.
Un dispositivo elettrocromico efficace avrà un passaggio rapido tra lo stato “on” e “off”, una buona durata caratterizzata da un lungo ciclo di vita e un elevato rapporto di contrasto ottico. Queste caratteristiche derivano, in parte, dalle proprietà del materiale elettrocromico attivo.
Molti fattori possono influenzare la velocità di commutazione come la conduttività elettronica dei materiali degli elettrodi e degli strati conduttori sottostanti, la conduttività ionica dell’elettrolita, la morfologia dello strato elettrocromico e i cambiamenti associati alla diffusione ionica all’interno di tale morfologia e alla cinetica di inserzione ionica.
La durabilità viene generalmente quantificata misurando i cambiamenti nella capacità di carica o nell’efficienza della colorazione nel corso di molte migliaia di cicli elettrochimici. L’ossido di tungsteno è il materiale elettrocromico più ampiamente studiato. Dopo l’iniezione di carica catodica faradaica, esso cambia colore da uno stato chiaro e trasparente a uno stato blu scuro e traslucido quando gli ioni di tungsteno vengono ridotti
I protoni o i cationi di metalli alcalini nell’elettrolita compensano gli elettroni iniettati attraverso l’inserimento nei siti ottaedrici dell’ossido di tungsteno e si ritiene che gli elettroni iniettati occupino la banda d precedentemente vuota, dando origine a nuove transizioni elettroniche.
Gli altri ossidi di metalli di transizione con colorazione catodica studiati sono TiO2, Nb2O5 , MoO3 e Ta2O5 . Gli ossidi con colorazione anodica vengono solitamente impiegati come controelettrodo che colora in modo complementare all’elettrodo elettrocromico primario. Il più noto di questi è il NiO, che è trasparente allo stato ridotto e grigio allo stato ossidato. Altri ossidi comunemente usati per la colorazione anodica sono IrO2 e V2O5.



