L’ossalato di calcio è un sale di calcio dell’acido ossalico avente formula CaC2O4 che può presentarsi monoidrato, triidrato e raramente biidrato.
Si presenta come un solido cristallino di colore bianco scarsamente solubile in acqua con un valore del prodotto di solubilità Kps pari a 2.7 · 10-9.
Una soluzione contenente ossalato di calcio ha un pH lievemente basico a causa dell’idrolisi dello ione ossalato inferiore a quello di una soluzione di ossalato di sodio a causa della maggiore solubilità di quest’ultimo.
Può essere trovato in qualsiasi tessuto o organo delle piante e spesso si forma nei vacuoli di cellule specializzate chiamate idioblasti cristallini. Lavori recenti indicano che la formazione di ossalato di calcio è generalmente un meccanismo per regolare i livelli di calcio libero nei tessuti e negli organi
È contenuto in molte piante come rabarbaro, cannella, curcuma e filodendro per le quali costituisce un elemento di difesa contro il loro consumo alimentare.
Sintesi dell’ossalato di calcio
Costituisce un intermedio della sintesi dell’acido ossalico.
Nel primo stadio avviene la reazione tra idrossido di calcio e ossalato di sodio con formazione di ossalato di calcio e idrossido di sodio:
Ca(OH)2 + Na2C2O4 → CaC2O4 + 2 NaOH
Nel secondo stadio, per ottenere l’acido ossalico, si acidifica la soluzione con acido solforico e si ha la formazione di acido ossalico e solfato di calcio:
CaC2O4 + H2SO4 → CaSO4 + H2C2O4
Decomposizione termica
Mediante analisi termogravimetrica (TGA) si possono avere informazioni relative alla decomposizione termica dell’ossalato di calcio idrato.
L’ossalato di calcio monoidrato così come quello biidrato si decompongono in tre stadi:
- alla temperatura di 115°C si ha la perdita di acqua con formazione dell’ossalato di calcio anidro:
CaC2O4·H2O → CaC2O4 + H2O
- a una temperatura di 425°C l’ossalato di calcio si decompone in carbonato di calcio e monossido di carbonio:
CaC2O4 → CaCO3 + CO
- a circa 600°C inizia la decomposizione del carbonato di calcio in monossido di calcio e biossido di carbonio:
CaCO3 → CaO + CO2
Calcoli di ossalato di calcio
I calcoli renali, noti anche come calcoli nelle vie urinarie, sono masse solide formate da minerali e sali che si sviluppano all’interno dei reni o delle vie urinarie. Queste formazioni possono variare in dimensioni e composizione e possono causare dolore intenso quando si spostano attraverso il tratto urinario.
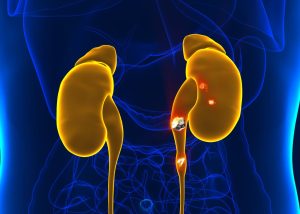
Circa il 10% della popolazione italiana è affetta da calcoli renali molti dai quali sono costituiti da ossalato di calcio. Il calcolo renale si forma quando la concentrazione di determinati ioni, nella fattispecie Ca2+ e C2O42- è tale da determinare la formazione dei primi cristalli che, aggregandosi tra loro, danno luogo alla formazione di piccoli sassolini.
Fonti
Lo ione ossalato è presente in molti alimenti tra cui:
- spinaci e altre verdure a foglia verde
- rabarbaro
- crusca di frumento
- mandorle
- barbabietole
- cioccolato
- patate fritte e al forno
- noci
- prodotti a base di soia
- fragole e lamponi
- tè
Lo ione calcio è largamente diffuso in molti alimenti di uso quotidiano tra cui:
