Glutatione perossidasi: protezione cellulare dall’ossidazione
La glutatione perossidasi (GPx) è il nome di una famiglia di enzimi della classe delle ossidoreduttasi scoperta dal biochimico Gordon C. Mills docente presso l’University of Texas Medical Branch nel 1952. Inizialmente fu attribuita a tale enzima un’attività nel proteggere l’emoglobina dalla degradazione ossidativa.
Negli anni ’60 l’attività del glutatione perossidasi è stata rilevata in altri tessuti ed è stato dimostrato che catabolizza gli idroperossidi organici oltre il perossido di idrogeno. Nel 1973 si scoprì che il selenio era essenziale per l’attività della glutatione perossidasi del fegato di ratto e si determinò che l’enzima purificato conteneva un atomo di selenio per subunità. Fu così identificata la prima selenoproteina animale nota oggi come GPX1 e, pochi anni dopo, si determinò che il selenio nella glutatione perossidasi era sotto forma di selenocisteina.
Dagli anni ’80 sono state scoperte altre glutatione perossidasi fino a un totale di otto e numerate da uno a otto di cui GPX4, GPX7 e GPX8 sono monomeri mentre i rimanenti sono omotetrameri ovvero costituiti da quattro monomeri identici tra di loro.
Antiossidanti e glutatione perossidasi
Gli antiossidanti sono sostanze che prevengono, riducono o ritardano l’ossidazione di specie che possono essere ossidati come proteine, lipidi, carboidrati e DNA nelle cellule viventi e pertanto prevengono o ritardano il danno dei radicali liberi dell’ossigeno sui tessuti bersaglio. Gli antiossidanti sono classificati in due categorie, enzimatici e non enzimatici.
Quelli enzimatici sono la superossido dismutasi, la catalasi e la glutatione perossidasi, mentre gli antiossidanti non enzimatici sono la vitamina E, la vitamina C, la vitamina A, il selenio, la transferrina e la lattoferrina.
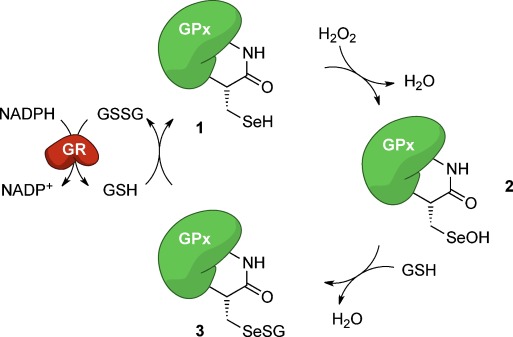
La glutatione perossidasi, che contiene il selenio nel suo centro attivo, è presente nel citosol e nei mitocondri e riduce non solo il perossido di idrogeno ma anche i perossidi lipidici.
Catalizza la reazione tra il glutatione (GSH), tripeptide con proprietà antiossidanti, costituito da cisteina e glicina, legate da un legame peptidico, e glutammato legato alla cisteina con un legame isopeptidico tra il gruppo carbossilico della catena laterale del glutammato e il gruppo amminico della cisteina e il perossido di idrogeno.
La reazione catalizzata è:
2 GSH+ H2O2 ⇄ GSSG + 2 H2O
Dove GSSG è il glutatione disolfuro che ha una ridotta capacità di ridurre il perossido. Una volta ossidato, il GSH può essere rigenerato dal GSSG dall’enzima glutatione reduttasi GR, utilizzando la nicotinammide adenina dinucleotide fosfato NADPH come donatore di elettroni.
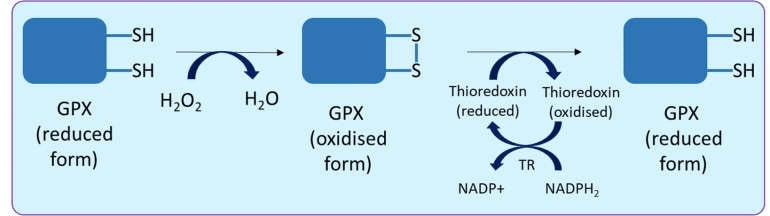
Nel processo, la NADPH viene ossidato a NADP + e NADPH è rigenerato attraverso la via dei pentoso fosfati . Pertanto, il ciclo redox dipendente dalla glutatione perossidasi, funziona come un meccanismo antiossidante cellulare.
Analoga reazione avviene con i perossidi lipidici LOOH:
2 GSH+ LOOH ⇄ GSSG + LOH + H2O
Glutatione perossidasi e stress ossidativo
Lo stress ossidativo è una condizione in cui si verifica uno squilibrio tra la produzione di specie ossidanti e la loro eliminazione da parte del sistema di difesa antiossidante.

Lo stress ossidativo è dovuto principalmente alle specie reattive dell’ossigeno (ROS). I ROS sono un gruppo di sostanze chimiche altamente reattive contenenti ossigeno derivanti dall’ossigeno molecolare.
Molti processi biologici come respirazione, digestione e trasformazione dei lipidi in energia producono radicali liberi. Questi ultimi sono solitamente distrutti dal sistema antiossidante naturale del nostro corpo. I radicali liberi, se questo sistema non funziona correttamente, possono innescare una reazione a catena.
ROS acronimo di Reactive Oxygen Species sono molecole chimiche o radicali liberi altamente reattivi.
Esempi di ROS sono:
- radicale idrossile HO∙
- radicale idroperossido HO2∙
- anione superossido ·O2–
- ozono O3
- perossido di idrogeno H2O2
Sebbene noti da molti decenni è solo negli ultimi tempi che è stato scoperto il loro ruolo nello sviluppo di malattie e, quindi, ampiamente studiati gli effetti benefici degli antiossidanti.
La glutatione perossidasi ha effetti antiossidanti nei sistemi biologici e biochimici ed è uno dei componenti del sistema di difesa antiossidante che protegge la cellula dal danno ossidativo dei radicali liberi o di altre molecole reattive. Gli effetti dannosi dei radicali liberi sono controllati dai sistemi di difesa antiossidante nelle cellule



