Il ruolo dei catalizzatori nella velocità delle reazioni chimiche
I catalizzatori accelerano le reazioni chimiche riducendo l’energia di attivazione e aumentando l’efficienza dei processi industriali.
Essi accelerano la velocità di una reazione termodinamicamente favorita portando a una diminuzione dell’energia di attivazione e, pur partecipando alla reazione non compaiono né tra i reagenti né tra i prodotti, e sono ritrovati inalterati alla fine di essa.
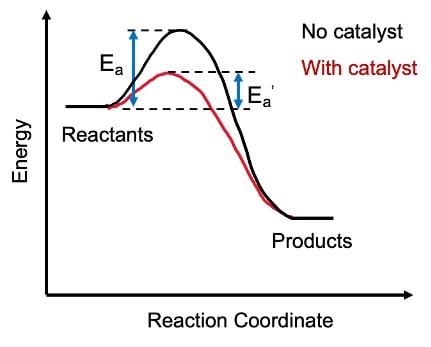
Il catalizzatore, riducendo l’energia di attivazione richiesta per avviare la reazione, crea una via reattiva alternativa che consente una maggiore velocità di reazione ovvero fornisce un percorso più favorevole perché la reazione avvenga, senza subire alterazioni chimiche permanenti.
La chimica è una scienza che si occupa dello studio delle trasformazioni della materia e delle reazioni chimiche che ne conseguono. Uno degli aspetti fondamentali da comprendere è la velocità con cui queste reazioni avvengono.
In accordo con la teoria delle collisioni proposta da Max Trautz e William Lewis nel 1916 affinché avvenga una reazione i reagenti devono collidere tra loro secondo una determinata orientazione in modo che possano rompersi i legami tra i reagenti e possano formarsi i legami nei prodotti della reazione.

Una reazione termodinamicamente favorita per la quale la variazione di energia libera è minore di zero può avvenire in tempi rapidi o in tempi più o meno lunghi. La velocità di una reazione chimica dipende da una serie di fattori quali la temperatura, la presenza di luce, la pressione, l’elettricità, il pH, la superficie di contatto tra i reagenti, lo stato fisico, la concentrazione e la presenza di catalizzatori.
Questi composti chimici sono in grado di accelerare le reazioni chimiche, consentendo un risparmio energetico e un aumento dell’efficienza dei processi industriali.
Meccanismo di azione dei catalizzatori eterogenei
I catalizzatori possono agire secondo diversi meccanismi, a seconda della natura della reazione chimica e delle caratteristiche del catalizzatore stesso. Uno dei meccanismi più comuni è quello della catalisi eterogenea, in cui il catalizzatore è in una fase diversa rispetto ai reagenti.
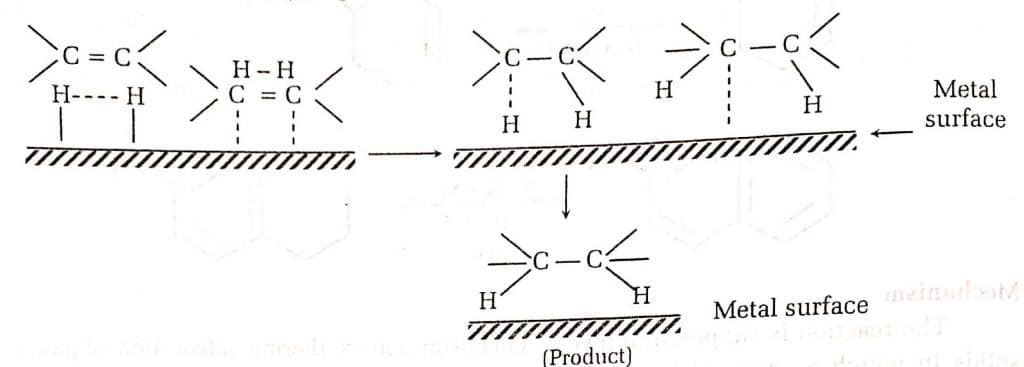
Ad esempio, le reazioni di idrogenazione sono realizzate generalmente in fase eterogenea e in presenza di catalizzatore in quanto pur essendo in genere favorite da un punto di vista termodinamico non lo sono da un punto di vista cinetico stante la forza del legame tra i due atomi di idrogeno presenti nella molecola di H2.
Per accelerare il decorso della reazione o si deve operare ad elevate temperature o si può usare un catalizzatore come rutenio, palladio, cobalto, rodio, platino, Nichel Raney sebbene quest’ultimo e richieda, rispetto ai precedenti, pressioni più elevate.
Le caratteristiche che deve presentare un catalizzatore eterogeneo sono: elevata attività, alta selettività, possibilità di riciclo. L’attività e la selettività dipendono dalla scelta del metallo che influenza la forza di adsorbimento dei reagenti, la velocità di desorbimento dei prodotti di reazione e la velocità delle trasformazioni chimiche.
Il catalizzatore solido fornisce una superficie sulla quale i reagenti possono essere adsorbiti e reagire più facilmente, accelerando così la reazione. La capacità di superfici solide di formare e rompere legami con le molecole, è alla base del fenomeno catalisi eterogenea di importanza industriale. La catalisi eterogenea è oggi uno dei processi industriali più importanti nella fabbricazione di sostanze chimiche
Si basa su reazioni superficiali, che richiedono l’adsorbimento di almeno uno dei reagenti sulla superficie del catalizzatore che sono spesso specifici per una particolare reazione, specificità che è tipica degli enzimi che sono dei catalizzatori biologici.
La ricerca si rivolge alle caratteristiche dei catalizzatori in relazione alle loro funzioni nel corso delle reazioni chimiche. Quando si riesce a trovare il catalizzatore adatto si possono spesso variare le condizioni di reazione rispetto a quelle con cui veniva condotta la reazione in assenza di catalizzatore.
Meccanismo di azione dei catalizzatori omogenei
Un altro meccanismo importante è la catalisi omogenea, in cui sia il catalizzatore che i reagenti sono presenti nella stessa fase. In questo caso, il catalizzatore forma complessi temporanei con i reagenti, stabilizzando le specie reattive e abbassando l’energia di attivazione necessaria per la reazione.
Dopo aver accelerato la reazione, il catalizzatore viene rigenerato e può partecipare ad altre reazioni. La reazione di ossidoriduzione:
VIII + FeII → VIV + FeIII
risulta catalizzata dalla presenza di ioni CuII .
Tale è un esempio di catalisi omogenea in fase liquida dato che tutte le specie partecipanti, compreso il catalizzatore, si trovano in soluzione. Un esempio di catalisi omogenea in fase gassosa è costituito dalla degradazione dell’ozono ad opera del cloro atomico secondo la reazione:
Cl + O3 → ClO + O2
Tra le catalisi omogenee di importanza industriale si ricorda la sintesi delle aldeidi dagli alcheni per idroformilazione e il processo Wacker per la sintesi dell’acetaldeide.



