Acido tungstosilicico
L’acido tungstosilicico o acido silicotungstico è un eteropoliacido con la formula chimica H4SiW12O40 che si presenta solitamente sotto forma idrata H4SiW12O40· n H2O. Gli eteropoliacidi (HPAs) sono degli acidi inorganici forti con ben definite strutture molecolari costituiti da ossiacidi inorganici di fosforo, silicio, e da quelli di tungsteno, molibdeno e vanadio.

Esempi di eteropoliacidi sono, insieme all’acido tungstosilicico, l’acido fosfotungstico H3PW12O40, e l’acido fosfomolibdico H3PMo12O40. La formula dell’acido tungstosilicico può essere scritta come 2 H2O·SiO2·12 WO3· n H2O.
A seconda del numero di molecole di acqua presenti nella struttura, l’acido tungstosilicico cristallizza secondo diversi reticoli. Cristallizza secondo in reticolo ottaedrico se n = 30, romboedrica se n = 24 e sotto forma di cristallo triclino se n = 22.
Struttura dell’acido tungstosilicico
La struttura dell’acido tungstosilicico è tipicamente quella di Keggin rappresentabile come [XM12O40]n- dove, in questo caso X è il silicio tetravalente e M è il molibdeno. Gran

parte della moderna chimica degli eteropoliacidi è incentrata sulla struttura Keggin dovuta al dottor James Fargher Keggin che, sotto la supervisione di William Lawrence Bragg e di Linus Pauling, pubblicò nel 1933 la struttura dell’acido fosfotungstico.
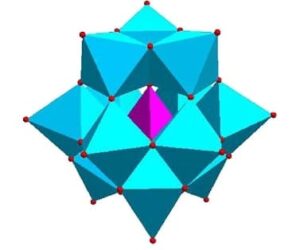
La struttura è costituita da una specie tetraedrica in cui al centro si trova l’eteroatomo e ai vertici quattro atomi di ossigeno. La struttura è costituita da dodici ottaedri {MO6} raggruppati in tre terne di {M3O15} che si legano in modo condiviso attorno all’unità centrale {XO4}. La struttura dimostrata, da Keggin per dell’acido fosfotungstico si è estesa anche all’acido tungstosilicico e all’acido fosfomolibdico
Sintesi
Tipicamente l’acido acido tungstosilicico viene sintetizzato dalla reazione tra il silicato di sodio e l’ossido di tungsteno (VI) in presenza di acido cloridrico secondo la reazione:
Na2SiO3 + 12 WO3 + 2 HCl + n H2O→ H4SiW12O40· (n-1) H2O + 2 NaCl
Stante il crescente interesse per l’acido tungstosilicico sono allo studio altre vie sintetiche. Una tra queste utilizza, quale precursore, il paratungstato di ammonio (NH4)10 (H2W12O42)· n H2O che è considerato il materiale di partenza per ottenere tutti i prodotti contenenti tungsteno.
A seguito di agitazione e regolando opportunamente il pH si ottiene il metatungstato di ammonio (NH4)6 (H2W12O42)· n H2O. A seguito dell’aggiunta di acido metasilicico, in presenza di ammoniaca e a un pH compreso tra 7 e 8 si ottiene (NH4)4 (SiW12O40) che viene fatto fluire in resine a scambio ionico per dare acido tungstosilicico.
Usi
Uno dei più noti e sperimentati usi dell’acido tungstosilicico in qualità di catalizzatore è nella reazione tra etene e acido acetico che, a seguito di alchilazione dà luogo alla formazione di acetato di etile:
C2H4 + CH3COOH → CH3COOCH2CH3
È utilizzato in qualità di catalizzatore anche nell’ossidazione dell’etene ad acido acetico:
C2H4 + O2 → CH3COOH
L’acido tungstosilicico, con la sua vasta gamma di applicazioni, ha un ruolo fondamentale nella ricerca scientifica. Questo acido è utilizzato nelle reazioni catalitiche, funge da reagente per la sintesi di composti organici e da catalizzatore per l’ossidazione delle sostanze organiche.
Esso inoltre, contribuisce alla produzione di prodotti farmaceutici e alla produzione di wafer di silicio di elevata purezza. L’acido tungstosilicico trova impiego anche nell’ottenimento di pigmenti, coloranti e vari prodotti industriali.
Al centro della sua versatilità risiede l’attività catalitica dell’acido tungstosilicico in numerose reazioni chimiche. Esso è utilizzato per catalizzare l’ossidazione dei composti organici come, ad esempio, alcoli, aldeidi e chetoni. Inoltre, agevola l’idrolisi di esteri e ammidi, nonché la condensazione di aldeidi e chetoni.
L’acido tungstosilicico è in grado di catalizzare la disidratazione degli alcoli e la polimerizzazione delle olefine. Sfruttando il potenziale catalitico dell’acido tungstosilicico, ricercatori e chimici possono sperimentare nuovi percorsi per la sintesi di composti organici, ottenere processi di ossidazione mirati e ottimizzare le procedure di produzione.
L’acido tungstosilicico, unitamente agli eteropoliacidi è stato inoltre recentemente indicato come catalizzatore eterogeneo e omogeneo versatile, rispettoso dell’ambiente, stabile ed ecologico per una varietà di reazioni organiche.



