Silicato di sodio
Il silicato di sodio è il più importante dei silicati solubili che potrebbe essere stato prodotto già dagli antichi egizi oltre 5000 anni fa attraverso la fusione di sabbia silicea e carbonato di sodio. I silicati solubili furono utilizzati da alcuni alchimisti del XVII secolo, come descritto nelle opere di Glauber e Agricola, ma è solo con gli studi e le produzioni industriali del XIX secolo che questa categoria di composti trovò sviluppo nelle varie e numerose le applicazioni.
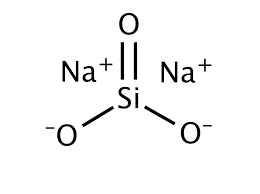
La formula del silicato di sodio è (Na2O)x(SiO2) essendo costituito da ossido di sodio e biossido di silicio in varie proporzioni. Quando il rapporto è di 1:1 la formula è Na2SiO3 e tale composto, che forma diversi sali idrati, è detto anche metasilicato di sodio. Utilizzando diverse proporzioni degli ossidi si hanno formula che vanno da Na2O · 4 SiO2 al silicato colloidale 2 Na2O · SiO2.
Il metasilicato di sodio, detto anche vetro solubile, una volta solubilizzato in acqua, forma una soluzione alcalina. Nelle soluzioni alcaline e neutre è completamente stabile ma, in soluzione acida gli ioni H+ reagiscono con lo ione SiO32- per dare acido ortosilicico da cui si può ottenere il gel di silice o silice colloidale utilizzato, per le sue proprietà adsorbenti, come essiccante, deumidificante, agente disidratante, adsorbente e riempitivo.
Sintesi del silicato di sodio
Le soluzioni di silicato di sodio possono essere ottenute attraverso diverse vie sintetiche trattando il biossido di silicio sotto forma di polvere di quarzo con idrossido di sodio in presenza di vapore secondo la reazione:
SiO2 + 2 NaOH → Na2SiO3 + H2O
Un’altra via sintetica prevede il trattamento di carbonato di sodio e biossido di silicio allo stato fuso:
Na2CO3 + SiO2 → Na2SiO3 + CO2
Il silicato di sodio può essere anche ottenuto dalla reazione tra solfato di sodio e biossido di silicio in presenza di carbonio che agisce quale agente riducente. Dalla reazione si ottiene anche biossido di carbonio e anidride solforosa:
Na2SO4 + C + SiO2 → Na2SiO3 + CO2 + SO2
Può essere ottenuto quale sottoprodotto nel processo Bayer in cui si ottiene l’ossido di alluminio a partire dalla bauxite.
Sintesi verde
La sintesi verde persegue la fattibilità di processi ad alta efficienza energetica per prevenire la formazione di rifiuti, utilizzare solventi più sicuri e sostanze chimiche rinnovabili e produrre materiali meno pericolosi con bassa tossicità.
Questa metodologia sintetica, realizzata con tecniche di sintesi affidabili, sostenibili ed ecologiche rispettando i 12 principi della Chimica verde formulati da Paul T. Anastas e John C. Warner nel 1991, ha ricevuto molta attenzione nel campo delle nanotecnologie in quanto affidabile, sostenibile e rispettosa dell’ambiente per la sintesi di un’ampia gamma di nanomateriali.
Attualmente per produrre il silicato di sodio si utilizza la silice estratta dalla sabbia o dal quarzo. Tuttavia la silice può essere estratta anche dagli scarti agricoli come la cenere di bagassa di canna da zucchero (SCBA) o la lolla di riso (RH) tramite metodi sostenibili come il trattamento termico che consente la rimozione di eventuali componenti organiche.
Applicazioni
Il silicato di sodio se utilizzato su superfici in calcestruzzo, agisce come sigillante, creando una solida barriera che protegge efficacemente dall’umidità e da altri elementi esterni. Il silicato di sodio reagisce con il l’idrossido di calcio presente nel cemento e con l’acqua dà luogo alla formazione di silicato di calcio idrato.

Il silicato di sodio è ampiamente utilizzato nella ceramica come agente legante ed è particolarmente utile per legare particelle di argilla fine o sabbiosa in quanto reagisce con la silice libera presente nell’argilla quando cotta ad alte temperature, formando un forte legame che conferisce alla ceramica una maggiore durevolezza e stabilità. Nel campo delle ceramiche l’uso del silicato di sodio può anche aiutare a prevenire crepe e restringimenti durante il processo di essiccazione.
Per le sue proprietà peculiari il silicato di sodio può essere utilizzato nei campi più svariati: l’aggiunta di una piccola quantità agli impianti di trattamento delle acque o agli impianti di trattamento delle acque reflue consente la flocculazione e i metalli pesanti affondano sul fondo del serbatoio.
Il trattamento di molte superfici compreso il legno con silicato di sodio conferisce all’oggetto un livello di controllo passivo del fuoco. Per i materiali utilizzati all’esterno funge da barriera per il controllo passivo degli insetti. Per le sue proprietà basiche è ideale per rimuovere oli e grassi, scomporre proteine e amidi e neutralizzare gli acidi quindi può essere usato sia nei detersivi per piatti che in quelli per bucato.

È utilizzato quale adesivo per carta, vetro, pelle, scatole e cartoni e specificamente usato in situazioni che comportano calore elevato, come la cottura al forno o il contatto con una fiamma libera. Viene spesso utilizzato nei fluidi di perforazione per stabilizzare le pareti del pozzo evitandone il collasso.
Viene utilizzato, insieme al silicato di magnesio, per la riparazione delle marmitte: quando questi due sali sono disciolti in acqua formano una pasta densa che viene applicata sul punto da riparare. Quando la marmitta si riscalda evapora l’acqua in eccesso lasciando la pasta vetrosa a sigillare, anche se in modo temporaneo, la marmitta.
Il silicato di sodio può essere un ottimo precursore per la sintesi di nanoparticelle di silice. Inizialmente, il silicato di sodio viene sciolto in acqua distillata e agitato a temperatura ambiente aggiungendo acido cloridrico. Le nanoparticelle vengono poi recuperate a seguito di filtrazione.
La silice porosa può essere ottenuta da soluzioni di silicato di sodio. Questa forma di silice porosa, ha tipicamente una dimensione media dei pori di 30 nm e un’area superficiale specifica BET di 5-100 m2 g-1.
Durante un tipico processo di precipitazione vengono aggiunti acido solforico e silicato di sodio ad una soluzione di acqua già contenente silicato di sodio la cui presenza aiuta a tamponare l’aggiunta iniziale dell’acido alla miscela di reazione. Le reazioni di condensazione dell’acido silicico che dipendono dal pH.
In presenza di un catalizzatore acido, i monomeri si condensano per formare strutture oligomeriche che vengono mantenute in soluzione tramite solvatazione. Alla fine queste molecole solvatate diventano abbastanza grandi da formare particelle solide e si forma una sospensione colloidale. Le particelle colloidali continuano a crescere per aggiunta di monomeri portando alla formazione di nanoparticelle.



