Indolo: aromaticità, proprietà, sintesi
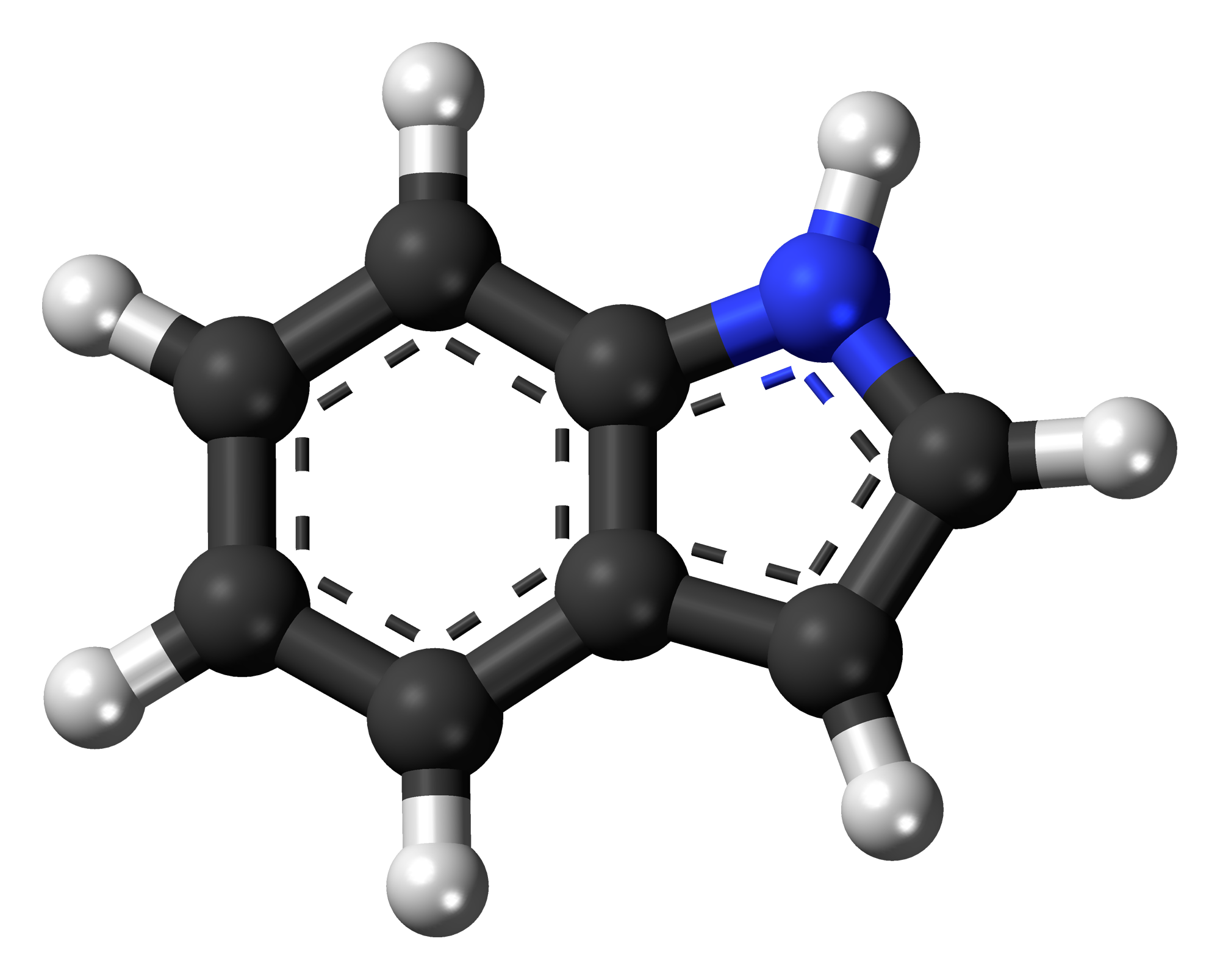
L’indolo è un eterociclo aromatico risultante dalla condensazione di un anello benzenico sulle posizioni α e β del pirrolo avente formula C8H7N.
L’aromaticità dell’indolo è dovuta al fatto che oltre ai tre doppi legami presenti nell’anello benzenico e al doppio legame presente nel pirrolo per un totale di 6 + 2 = 8 elettroni vi è anche il doppietto elettronico solitario dell’azoto che contribuisce alla nuvola elettronica π che è costituito così da un totale di 10 elettroni e rispetta la regola di Huckel per la quale sistemi ciclici planari con una nuvola π ininterrotta contenenti elettroni π in numero di 4n + 2 dove n è un numero intero sono aromatici.
Proprietà dell’indolo
A causa della sua aromaticità è scarsamente basico a causa del coinvolgimento della coppia solitaria dell’azoto incorporato nella risonanza della struttura biciclica aromatica.
Il chimico tedesco Johann Friedrich Wilhelm Adolf von Baeyer nell’ambito dei suoi studi sul colorante indaco sintetizzò per la prima volta questo eterociclo.

L’indolo è prodotto dalla degradazione del triptofano insieme allo scatolo che è un suo β-metil-derivato è responsabile dell’odore delle feci.
A basse concentrazioni, invece, è il responsabile di alcuni odori floreali come quello di gelsomino, di fiori di arancio e di Robinia pseudoacacia e trova pertanto utilizzo nel campo dei profumi.
L’indolo è inoltre contenuto nelle frazioni altobollenti del catrame di carbon fossile.
Sintesi
L’indolo e i suoi derivati possono essere ottenuti attraverso molte vie sintetiche tra cui la sintesi di Fischer. In essa è fatta reagire la fenilidrazina e un’aldeide o un chetone in ambiente acido:
Questa sintesi può tuttavia portare solo a derivati dell’indolo. Invece se si vuole ottenere l’indolo o i suoi derivati si può ricorrere alla sintesi di Madelung tramite una ciclizzazione intramolecolare di una N-fenilammide in presenza di una base forte e elevate temperature.
La posizione 3 dell’indolo è la più reattiva nei confronti di un elettrofilo; tramite la reazione di Mannich si ottengono quindi indoli sostituiti in posizione 3 tra cui le gramine, alcaloidi indolici ad azione calmante
Gli alcaloidi indolici di cui il triptofano è spesso il precursore sono numerosi e con diverse e molteplici azioni biologiche. Sono estratti da diverse piante appartenenti alla famiglia delle Apocinaceae, Rubiaceae, Leguminosae, Loganiaceae e da funghi delle Clavicipitaceae.
Alcaloidi indolici sono:
- reseprina con attività antipertensiva
- vinblastina utilizzata nella terapia di alcuni tumori
- fisostigmina utilizzata per la sua caratteristica di inibitore reversibile dell’acetilcolinesterasi
- ergotamina principio attivo di indicazione specifica per il trattamento dell’emicrania
- yoimbina che ha effetti stimolanti sul sistema nervoso centrale.
Reazioni
L’anello indolico può partecipare ad un’ampia gamma di reazioni chimiche, in particolare in C3, ad esempio sostituzione elettrofila, litiazione del carbonio, ossidazione e cicloaddizione. Inoltre, gli indoli possono essere coinvolti in una varietà di reazioni biochimiche come la formazione di spore, la stabilità dei plasmidi, la formazione di biofilm e la virulenza nei batteri.
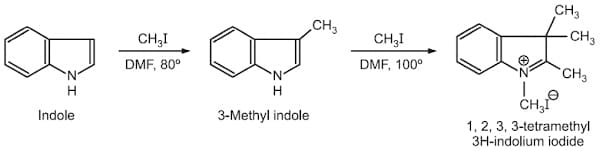
L’indolo dà reazioni di alchilazione reagendo con alogenuri alchilici come lo iodometano il presenza di dimetilformammide. Alla temperatura di 80°C si forma il 3-metilindolo mentre alla temperatura di 100°C dà luogo alla formazione del sale.
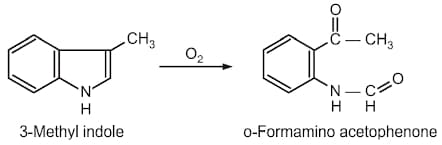
Quando è esposto all’aria o alla luce reagisce con l’ossigeno ossidandosi. Ciò porta alla rottura del doppio legame tra il carbonio 2 e il carbonio 3 con ottenimento di un amminoacetofenone.
L’indolo dà reazioni di riduzione: in
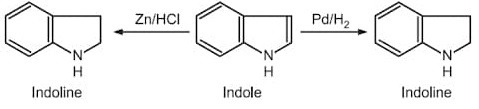
presenza di zinco e di acido cloridrico o, in alternativa, per idrogenazione catalitica in presenza di palladio si ha la rottura del doppio legame con formazione dell’indolina, costituita da un anello benzenico a sei membri fuso con un anello contenente azoto a cinque membri. Solo il litio, in presenza di ammoniaca, è in grado di ridurre anche l’anello aromatico.