Condensazione di Claisen–Schmidt
La condensazione di Claisen–Schmidt è una condensazione aldolica incrociata dovuta al chimico tedesco Rainer Ludwig Claisen e a J. Gustav Schmidt che pubblicarono l’esito delle loro ricerche, indipendentemente l’uno dall’altro, nel 1880 e nel 1881.
La condensazione di Claisen–Schmidt avviene tra un’aldeide aromatica che, come tale, non ha idrogeni in α al carbonile e un’aldeide alifatica con un idrogeno in α al carbonile o un chetone con un idrogeno in α al carbonile in presenza di una base forte come un idrossido o un alcossido da cui si ottiene un’aldeide o un chetone α,β-insaturo.
Attraverso la condensazione di Claisen–Schmidt, ad esempio, in ambiente basico la benzaldeide che non ha idrogeni α, non forma enolati e non può autocondensare, reagisce con l’acetone il cui equilibrio di autocondensazione è sfavorevole per dare il prodotto di doppia condensazione e disidratazione ovvero l’ 1,5-difenil-1,4-pentadien-3-one noto come dibenzalacetone spesso abbreviato come DBA.
Il DBA e i suoi analoghi, che possono essere sintetizzati da una classica condensazione di Claisen-Schmidt, sono strutturalmente simili ai calconi che sono considerati strutture privilegiate in chimica farmaceutica e sono una componente di alcuni farmaci commercializzati. In generale la condensazione di Claisen–Schmidt è una strategia sintetica nell’ambito della sintesi organica e nella biochimica per formare legami carbonio-carbonio.
Meccanismo della condensazione di Claisen–Schmidt
Nel primo stadio della condensazione di Claisen–Schmidt la base estrae l’idrogeno in α al gruppo carbonilico dell’aldeide o del chetone per formare un anione enolato stabilizzato per risonanza. Per la formazione di uno ione enolato è quindi necessaria la presenza di un chetone o un’aldeide enolizzabile. Tale reazione è quantitativa in presenza di basi forti.
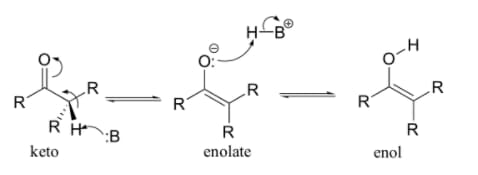
Spesso, come nella condensazione di Claisen–Schmidt, nella reazione di Mannich e nelle condensazioni aldoliche, gli enolati vengono generati in basse concentrazioni con basi alcossidiche ma possono comunque dare reazioni con gli elettrofili.
Quando un enolato si forma da un’aldeide, esso reagisce con l’aldeide non reagita per dare una reazione di condensazione aldolica. Poiché i chetoni sono meno reattivi nei confronti dell’addizione nucleofila, l’enolato formato da un chetone può essere utilizzato per reagire con un’aldeide, tramite la condensazione di Claisen-Schmidt.
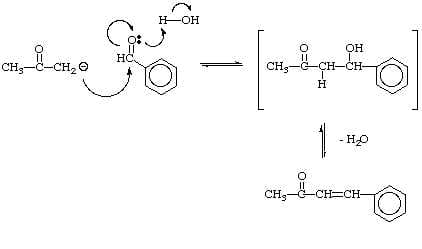
Nel secondo stadio della reazione l’enolato agisce da nucleofilo e attacca il carbonio carbonilico. Se il prodotto formato ha ancora un idrogeno α reattivo e un idrossido adiacente ad un anello aromatico, la reazione subirà rapidamente una disidratazione portando al prodotto di condensazione.
La condensazione di Claisen-Schmidt comporta sempre la disidratazione del prodotto misto di condensazione aldolica
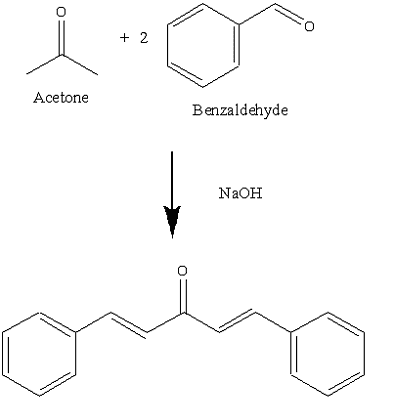
per produrre una sostanza chimica in cui il doppio legame prodotto durante la disidratazione è coniugato sia all’anello aromatico che al gruppo carbonilico.
In eccesso di aldeide aromatica la reazione si ripete in modo del tutto analogo in cui l’anione enolato agisce da nucleofilo nei confronti del carbonio carbonilico del prodotto formatosi nella prima reazione per dare il prodotto finale che, nel caso della reazione tra benzaldeide e acetone è il dibenzalacetone che è stato impiegata come bloccante dei raggi ultravioletti nelle preparazioni per la protezione solare.
Vantaggi
La reazione di condensazione aldolica è una delle reazioni importanti dei composti carbonilici e avviene in ambiente basico tra due molecole di aldeide o chetone aventi almeno un atomo di idrogeno in α al carbonile da cui si ottengono, rispettivamente una β-idrossi aldeide o un β-idrossi chetone.
La condensazione aldolica fatta con due diversi composti carbonilici sono chiamate condensazioni aldoliche incrociate. Se entrambe le molecole hanno protoni in α al carbonile allora si ottengono una miscela di prodotti con strutture simili che dovranno essere separati e le rese del prodotto desiderato saranno inferiori.
Affinché una condensazione aldolica incrociata sia sinteticamente utile una specie deve avere protoni in α al carbonile ovvero essere enolizzabile mentre l’altra specie non deve avere protoni in α al carbonile; in tal caso si ottengono chetoni α,β insaturi ovvero i prodotti della condensazione di Claisen-Schmidt



