Cicloottatetraene: struttura, proprietà, reazioni
Il 1,3,5,7-cicloottatetraene (COT) è un poliene ciclico coniugato non aromatico e non planare con formula C8H8 noto anche come [8]annulene
Esso non soddisfa la regola di Hückel infatti il numero di elettroni π pari a 8 e non a 4n+2. Per la struttura chimica planare , i calcoli di meccanica quantistica mostrano due degli orbitali molecolari di legame occupati da un elettrone ciascuno con momento di spin parallelo.
Questa struttura implica un’instabilità molto più elevata e ciò è stato osservato negli esperimenti.
Per la struttura non planare, i calcoli di meccanica quantistica mostrano un’altra disposizione in cui tutti gli orbitali molecolari di legame sono occupati da due elettroni.
Adotta una conformazione a barca non planare per raggiungere la stabilità presentando legami singoli e doppi alternati e quindi si comporta come una poliolefina

Proprietà
È un liquido di colore giallo chiaro immiscibile con l’acqua
I doppi legami non sono in risonanza poiché gli orbitali p dei doppi legami adiacenti non possono sovrapporsi. Infatti il calore di idrogenazione del cicloottatetraene è di 410 kJ/mol circa quattro volte maggiore rispetto al cicloottene per il quale ΔH = 97 kI/mol
Sintesi del cicloottatetraene
Il chimico tedesco Richard Martin Willstätter, vincitore del Premio Nobel per la Chimica nel 1915 per le sue ricerche sui pigmenti delle piante, sintetizzò nel 1905 il cicloottatetraene partendo da un alcaloide.
Tuttavia la reazione, che prevedeva quattro eliminazioni successive, presentava una scarsa resa, successivamente il chimico tedesco Walter Julius Reppe ottenne il prodotto con una resa del 90% partendo da acetilene per trattamento con cianuro di nichel, carburo di calcio a 60°C e 60 atm utilizzando quale solvente il tetraidrofurano
Reazioni
A causa della presenza di quattro doppi legami dà reazioni di addizione tipiche degli alcheni.
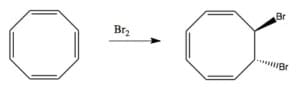
Ad esempio l’alogenazione porta alla rottura di un doppio legame e alla formazione di un dialogenuro vicinale
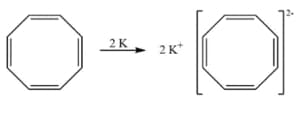
Reagisce con il potassio per formare il dianione aromatico [C8H8]2-
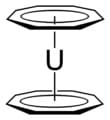
che funge da legante in alcuni metalloceni come l’uranocene.
È inoltre in grado di subire una varietà di reazioni di ossidazione e cicloaddizione per dare strutture policicliche
Usi
È utilizzato nella sintesi di film per superfici in silicio per migliorarne le proprietà chimiche e fisiche.
Può essere funzionalizzato da due gruppi laterali utilizzati come materiali anodici attivi per batterie ricaricabili.





