Gruppo metilenico
In chimica organica un gruppo metilenico è una parte di molecola costituita da due atomi di idrogeno e un atomo di carbonio legato, tramite legami semplici a due atomi di carbonio. Nel gruppo metilenico -CH2– il carbonio ha generalmente ibridazione sp3.
Il gruppo metilenico, formalmente derivante dal metano per allontanamento di due atomi di idrogeno, si differenzia dal gruppo metilico -CH3 in cui il carbonio ha comunque ibridazione sp3 e dal gruppo metilidene, spesso impropriamente detto metilene, in cui due atomi di idrogeno sono legati ad un atomo di carbonio, legato al resto della molecola da un doppio legame. Il gruppo metilidene, in cui il carbonio ha ibridazione sp2 e rappresentato come =CH2.
Il gruppo metilenico è presente in numerosi composti organici e, tipicamente negli alcani, ad esempio il propano CH3CH2CH3, negli alcheni, ad esempio l’1-butene CH2 =CH-CH2CH3, nei cicloalcani ma può essere trovato in aldeidi come ad esempio nella propionaldeide CH3CH2CHO, negli alcoli come l’etanolo CH3CH2OH ed in genere in tutti i composti costituiti da un elevato numero di atomi di carbonio.
Negli spettri di Risonanza Magnetica Nucleare scoperta indipendentemente nel 1946 dai fisici Felix Bloch ed Edward Purcell, per cui ricevettero il premio Nobel per la fisica nel 1952, il gruppo metilenico risuona, a seconda del suo intorno chimico a circa 3.5-4 ppm.
Gruppo metilenico attivato
I composti che contengono un gruppo metilenico legato a gruppi elettronattrattori come, ad esempio, il gruppo carbonilico, nitrile o nitro sono detti composti metilenici attivati. La presenza di gruppi elettronattrattori, infatti, rende acido un idrogeno legato al carbonio metilenico.

Ciò è dovuto alla stabilizzazione per risonanza dell’anione enolato che rende questi idrogeni più acidi cioè con valori di pKa più bassi rispetto agli idrogeni adiacenti a un singolo gruppo elettronattrattore. Pertanto gli atomi di idrogeno del gruppo metilenico sono significativamente acidi in quanto il carbanione ottenuto dall’allontanamento di un idrogeno è stabilizzato per risonanza.
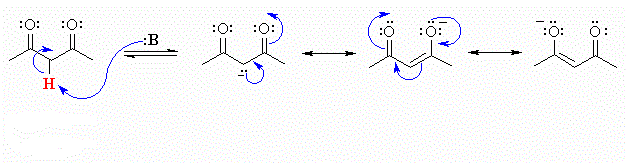
I composti che tipicamente presentano un metilene attivato sono i β-dichetoni, i β-chetosteri e i β-diesteri come, ad esempio, l’1,3-propandioato di dietile noto come malonato di etile. Conseguentemente questi composti sono acidi e possono essere irreversibilmente deprotonati con le basi come NaOH o con un alcossido.
Reazione di addizione di Michael
La reazione di addizione di Michael è un particolare tipo di reazione di addizione coniugata che i composti carbonilici ɑ, β -insaturi, ovvero composti bifunzionali caratterizzati dalla presenza di un doppio legame coniugato con un gruppo carbonilico che può essere di un chetone, di un’aldeide, di un estere, subiscono con i nucleofili. Appartiene alla classe più ampia delle addizioni coniugate ed è ampiamente utilizzata per la formazione di legami carbonio-carbonio in condizioni blande.
In generale, i composti carbonilici ɑ,β -insaturi possono subire una reazione di addizione 1,2 o 1,4. Le reazioni di addizione 1,2 sono tutte quelle in cui il nucleofilo attacca il gruppo carbonilico come la reazione dei composti carbonilici con un reattivo di Grignard o con un composto organico del litio.
A differenza dei composti metallorganici, nucleofili relativamente deboli come alogenuri, ioni cianuro, tioli, alcol e ammine, danno luogo all’addizione 1,4.
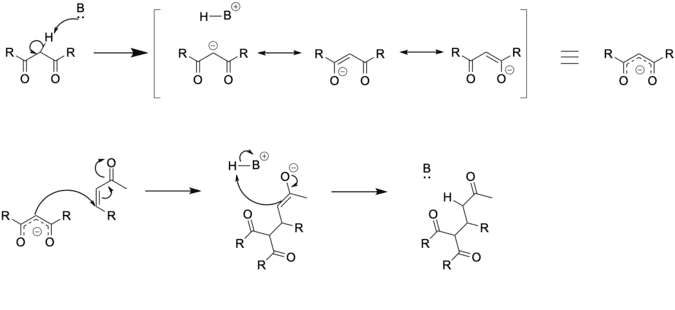
La reazione avviene tra un donatore di Michael costituito da un enolato o da un altro nucleofilo e un accettore di Michael solitamente un composto carbonilico α,β-insaturo per produrre un addotto di Michael. L’addizione di Michael è una reazione organica utilizzata per convertire un metilene attivato e un’olefina coniugata nel corrispondente prodotto di addizione utilizzando un catalizzatore basico seguito da una reazione con un acido.
Dopo la deprotonazione da parte della base di un idrogeno legato al carbonio metilenico attivato si forma un anione stabilizzato per risonanza che a sua volta dà luogo a un’addizione 1,4 all’olefina coniugata.



