Dimerizzazione degli alcheni
La dimerizzazione degli alcheni è un metodo per ottenere alcheni con un maggior numero di atomi di carbonio. I dimeri e gli oligomeri degli alcheni appartengono a una classe di composti molto richiesti in vari settori industriali. Tipicamente, vengono utilizzati come nella polimerizzazione dell’etilene e servono come materie prime per la produzione di adesivi, tensioattivi, aromi e additivi per combustibili sintetici
Il dimero è una molecola derivante dall’unione di due monomeri o per addizione o per condensazione
La dimerizzazione può avvenire a partire da un carbocatione
Un carbocatione infatti è anche una specie elettrofila e come tale può essere l’agente che conduce ad una reazione di addizione al doppio legame dell’alchene. Il caso più semplice di dimerizzazione è quella del 2 metil 1-propene.
In presenza di acido solforico concentrato, tale composto è trasformato in una miscela di due alcheni isomeri aventi complessivamente otto atomi di carbonio di cui il 2,4,4 trimetil 1 pentene con una resa dell’80% e il 2,4,4 trimetil 2 pentene.
Tra i metodi in via di sviluppo con un significativo potenziale di dimerizzazione degli alcheni c’è la catalisi della dimerizzazione e oligomerizzazione degli alcheni utilizzando sali e complessi metallici che forniscono elevate velocità di reazione e un controllo efficace della loro, regio e stereoselettività.
Meccanismo della dimerizzazione degli alcheni
Il meccanismo della reazione coinvolge tre stadi:
1) Addizione dello ione H+ derivante dalla dissociazione dell’acido solforico al 2- metil- 1 propene con formazione del carbocatione più stabile ovvero il carbocatione terziarbutilico.
2) Addizione del carbocatione ad un’altra molecola di alchene con formazione di un nuovo carbocatione a otto atomi di carbonio.
3) Perdita di un protone che comporta la formazione di un doppio legame con conseguente formazione del dimero.
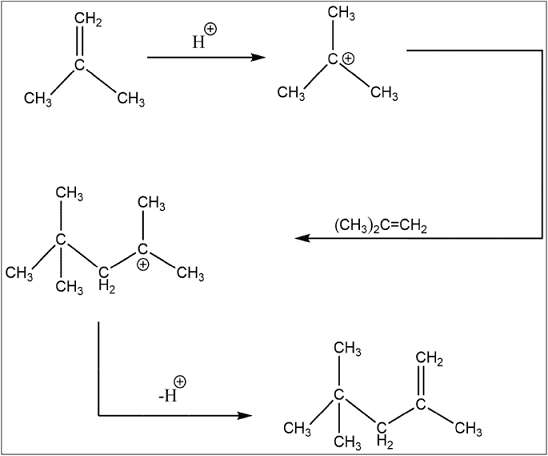
Il carbocatione terziario può perdere un protone da due differenti atomi di carbonio adiacenti portando così ai due alcheni isomeri.
La concentrazione dell’acido gioca un ruolo fondamentale in quanto se è troppo diluito il catione reagisce con l’acqua portando alla formazione del 2 metil propan-2-olo ovvero ad una tipica reazione di idratazione.
Se invece l’acido solforico è troppo concentrato esso non contiene nucleofili adatti a rimuovere il protone nello stadio 3) e conseguentemente il carbocatione a otto atomi può ulteriormente reagire con il 2 metil 1 propene.
Successivi stadi di addizione possono portare ad alcheni ad elevato peso molecolare ed in particolare a un polimero tramite un meccanismo di polimerizzazione cationica.



