Determinazione del glucosio
La determinazione del glucosio ha una grande importanza nella diagnostica clinica, nell’industria alimentare e nella biotecnologia. Pertanto sono stati messi a punto numerosi metodi strumentali per la determinazione del glucosio tra cui la cromatografia liquida ad alta prestazione (HPLC), metodi elettrochimici, spettrofotometria, fluorescenza, chemiluminescenza (CL) ed elettrochemiluminescenza (ECL).
Vi sono, tuttavia, numerosi metodi chimici per la determinazione del glucosio che si basano sul fatto che il glucosio è uno zucchero riducente che può reagire per dar luogo a precipitati o complessi colorati che possono essere quantificati.
Questi metodi per la determinazione del glucosio e, in generale, degli zuccheri riducenti possono essere di tipo volumetrici, colorimetrici oltre che tramite il saggio di Benedict, il metodo di Bertrand e quello di Hagedorn-Jenson.
Tra i metodi volumetrici per la determinazione del glucosio vi è la iodometria in cui il campione viene trattato con iodio che ossida il glucosio riducendosi a ioduro che è titolato con tiosolfato di sodio.
Determinazione del glucosio e iodometria
La iodometria si basa sull’ossidazione dello ioduro in iodio elementare secondo la semireazione: 2 I– ⇌ I2 + 2e– per la quale il potenziale normale di ossidazione E° = – 0.535 V. La iodometria è un metodo indiretto in cui viene aggiunto un eccesso di ioduro al campione contenente l’analita in soluzione acquosa.
La iodometria è utilizzata nell’analisi degli zuccheri riducenti, ovvero gli zuccheri che contengono un gruppo aldeidico –CHO, che può essere facilmente ossidato a gruppo carbossilico –COOH. Pertanto la determinazione del glucosio può essere fatta per via iodometrica
La reazione è quantitativa in ambiente basico, perché il gruppo carbossilico è acido e forma sali con basi. Il glucosio viene ossidato con iodio in soluzione alcalina e dopo acidificazione lo iodio in eccesso viene titolato con una soluzione di tiosolfato standardizzata usando la salda d’amido quale indicatore
Metodica
In una beuta si pongono 10 mL di analita a cui si aggiungono 10 mL di una soluzione standard 0.05 M di iodio e 10 mL di una soluzione di carbonato di sodio 1 M.
In ambiente basico lo iodio dà luogo a una reazione di dismutazione con formazione di ipoiodito e ioduro:
2 OH– + I2 → IO– + I– + H2O
Lo iodio infatti passa da numero di ossidazione 0 a numero di ossidazione +1 nell’ipoiodito e a numero di ossidazione -1 nello ioduro. Il gruppo aldeidico viene ossidato dall’ipoiodito che si trasforma in ioduro a gruppo carbossilico e, nello specifico, poiché l’ambiente è basico a gruppo carbossilato:
RCHO + IO– → RCOOH + I–
L’eccesso di ipoiodito in soluzione basica dà luogo a una reazione di dismutazione con formazione di iodato (incolore) e ioduro:
3 IO– → IO3– + 2 I–
Lo iodio infatti passa da numero di ossidazione +1 nell’ipoiodito a numero di ossidazione +5 nello iodato e -1 nello ioduro
La beuta viene coperta con un vetrino da orologio e la soluzione è fatta riposare al buio per 10 minuti. Si aggiungono quindi 10 mL di acido solforico 1 M prima di iniziare la titolazione per la determinazione del glucosio. Infatti in ambiente acido l’eccesso di iodato reagisce con lo ioduro tramite una reazione di comproporzione per dare iodio:
NaIO3 + 5 NaI + 3 H2SO4 → 3 I2 + 3 Na2SO4 + 3 H2O
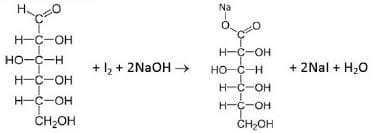
Lo iodio in ambiente basico reagisce con il glucosio in rapporto 1:1. Dalla reazione si ottiene ioduro e acido gluconico.
Lo iodio viene titolato con la soluzione con il tiosolfato fin quando, in prossimità del punto equivalente, diventa giallo pallido. Si aggiunge la salda d’amido e si titola fino a scomparsa del colore blu. Quando si effettua la titolazione la salda d’amido va infatti aggiunta in prossimità del punto finale ovvero quando è bassa la concentrazione di iodio che potrebbe essere adsorbito dall’indicatore.

La colorazione blu è poco visibile a elevati valori di pH e alte temperature. Le titolazioni sono quindi condotte a valori di pH minori di 8 e a temperatura ambiente.
Il tiosolfato reagisce con lo iodio per dare ioduro e tetrationato secondo la reazione:
2 S2O32- + I2 ⇌ S4O62– + 2 I–
Nota la concentrazione della soluzione di tiosolfato e il volume utilizzato per la titolazione si calcolano le moli. (moli di tiosolfato = concentrazione · volume in Litri). Poiché il rapporto tra tiosolfato e iodio è di 2:1 le moli di I2 sono pari alla metà di quelle di tiosolfato. Il rapporto tra glucosio e iodio è di 1:1 quindi le moli di I2 sono pari a quelle di glucosio.
Ruolo e fonti del glucosio
Il glucosio è un monosaccaride aldeidico che è fondamentale nei processi di fotosintesi e respirazione, fungendo da riserva energetica e combustibile metabolico nella maggior parte degli organismi. Sia come monomero che come parte di strutture più complesse come polisaccaridi e glucosidi, il glucosio svolge anche un ruolo importante nei prodotti alimentari.
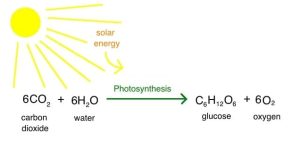
Nelle piante e nei cianobatteri, il glucosio viene prodotto dall’acqua e dall’anidride carbonica tramite la fotosintesi e condensato per formare amido. L’amido può essere immagazzinato come riserva energetica, oppure scomposto e utilizzato come substrato per la sintesi di un’ampia varietà di saccaridi, inclusi saccarosio e cellulosa. Negli alimenti, in particolare quelli di origine vegetale, questi diversi carboidrati contribuiscono notevolmente alla consistenza e al sapore, fungendo allo stesso tempo da fonte secondaria di energia.
A metà del XVIII secolo furono concepiti per la prima volta rudimentali test colorimetrici in grado di rilevare in modo non specifico gli zuccheri riducenti nel sangue e nelle urine. Sebbene sviluppati a scopo diagnostico e per il monitoraggio del diabete umano, questi metodi si sono rivelati ugualmente efficaci per la determinazione del glucosio negli estratti vegetali e nei prodotti alimentari come succhi e miele. Esso, unitamente ad altri monosaccaridi e disaccaridi, è spesso aggiunto agli alimenti per influenzarne le caratteristiche fisiche, oltre che la consistenza.
Gli zuccheri svolgono un ruolo importante nella cottura dei prodotti da forno in quanto interagisce con gli agenti lievitanti per creare piccole bolle d’aria e sono utilizzati quali conservanti in quanto aiutano a prevenire o rallentare la crescita di batteri, muffe e lieviti.
Gli zuccheri sono aggiunti ai prodotti da forno per conferire dolcezza ma anche il tipico colore che si forma quando reagiscono con le proteine durante il processo di cottura secondo la reazione di Maillard.



