Litio alluminio idruro: reazioni, sintesi
Il litio alluminio idruro ha formula LiAlH4 ed è un forte agente riducente non selettivo che costituisce un fonte di ioni idruro H–.
Le sostanze che agiscono da donatori di uno ione idruro sono caratterizzate dalla presenza di un atomo di idrogeno legato a un elemento meno elettronegativo.
Quanto maggiore è la differenza di elettronegatività tra l’idrogeno e l’altro elemento tanto più la sostanza è in grado di agire come donatore di uno ione idruro. E’ un solido bianco scoperto da Finholt, Bond e Schlesinger nel 1947
Reazioni del litio alluminio idruro
La specie che più delle altre risponde a questo requisito è il litio alluminio idruro che reagisce in modo violento con i solventi protici ed è pertanto utilizzato in solventi inerti come il dietiletere o il tetraidrofurano.
In presenza di acqua, infatti, dà luogo a una reazione con formazione di idrogeno:
LiAlH4 + 4 H2O → LiOH + Al(OH)3 + 4 H2
Il litio alluminio idruro dà luogo a una reazione di decomposizione termica in un meccanismo a tre stadi:
3 LiAlH4 → Li3AlH6 + 2 Al + 3 H2
2 Li3AlH6 → 6 LiH + 2 Al + 3 H2
2 LiH + 2 Al → 2 LiAl + H2
L’alluminio infatti ha una bassa elettronegatività rispetto all’idrogeno e il legame è covalente polare in cui l’alluminio ha una parziale carica positiva mentre l’idrogeno ha una parziale carica negativa.
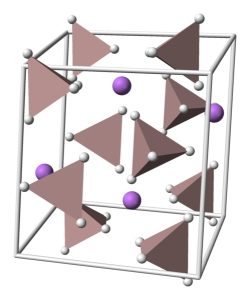
Il litio alluminio idruro è costituito dallo ione litio a dall’anione AlH4–. Quest’ultimo ha struttura tetraedrica con angoli di legame H-Al-H di 109.5°
Sintesi
Il litio alluminio idruro è preparato su piccola scala facendo reagire l’idruro di litio con il cloruro di alluminio:
4 LiH + AlCl3 → LiAlH4 + 3 LiCl
A livello industriale il litio alluminio idruro è preparato facendo reagire sodio, alluminio e idrogeno in condizioni di alta temperatura e alta pressione:
Na + Al + 2 H2 → NaAlH4
Nel secondo stadio della reazione il sodio alluminio idruro prodotto viene fatto reagire con cloruro di litio
NaAlH4+ LiCl → LiAlH4 + NaCl
Usi
Il litio alluminio idruro viene utilizzato nelle sintesi organiche quale agente riducente ed in particolare nella riduzione degli esteri e degli acidi carbossilici ad alcoli primari, nella riduzione degli alogenuri alchilici ad alcani, delle ammidi e dei nitrili ad ammine, degli epossidi ad alcoli e dei lattoni a diolo
Trova inoltre utilizzo quale catalizzatore nelle reazioni di polimerizzazione e quale propellente. Stante l’elevato contenuto di idrogeno si ritiene che possa costituire una sostanza potenzialmente utile nelle celle a combustibile.



