Blu di bromotimolo: indicatore acido-base
Il blu di bromotimolo è un indicatore acido-base comunemente utilizzato in laboratorio nelle titolazioni.
Esso infatti cambia colore in base all’acidità o alla basicità della soluzione in cui è disciolto. In soluzioni acide assume un colore giallo, mentre in soluzioni basiche assume un colore blu.
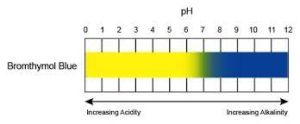
A pH neutro, la soluzione appare di colore verde. Il punto di viraggio del blu di bromotimolo si trova approssimativamente nell’intervallo di pH compreso tra 6.0 e 7.6. Il suo pKa è infatti pari a 7.1 ed è pertanto utilizzato nelle titolazioni in cui il pH al punto equivalente entra in questo range.

Pertanto si utilizza prevalentemente nelle titolazioni acido forte-base forte come, ad esempio acido cloridrico e idrossido di sodio, per le quali il pH al punto equivalente è pari a 7. Tuttavia, spesso è utilizzato in combinazione con il giallo di bromocresolo per creare una scala di colori che copre un’ampia gamma di pH.
Può anche essere utilizzato per monitorare la variazione di pH che avviene nel corso di un esperimento chimico o per osservare le attività fotosintetiche. Una soluzione contenente l’indicatore, infatti, per aggiunta di biossido di carbonio diventa gialla. Ciò è dovuto al fatto che l’anidride carbonica gassosa si solubilizza secondo l’equilibrio:
CO2(g) ⇄ CO2(aq)
Successivamente avviene la reazione tra il biossido di carbonio e l’acqua con formazione dell’acido carbonico:
CO2(aq) + H2O(l) ⇄ H2CO3(aq)
Pertanto è spesso utilizzato in piscine, acquari e, in generale, per misurare la presenza di acido carbonico in una soluzione. Una dimostrazione comune delle sue proprietà comporta l’espirazione attraverso un tubo in una soluzione neutra. Quando l’anidride carbonica è assorbita dalla soluzione, formando acido carbonico, la soluzione cambia colore da verde a giallo.
Proprietà del blu di bromotimolo
È un composto sintetico che appartiene alla classe dei tiazoli e ha la formula chimica C27H28Br2O5S. È generalmente solubile in solventi organici come l’alcool etilico, il metanolo, il cloroformio e l’acetone. Inoltre è anche solubile in soluzioni acquose alcaline, formando una soluzione blu.
Tuttavia, è poco solubile in acqua e può formare una sospensione o precipitare come cristalli fini in soluzioni acquose neutre o acide. È poco solubile in solventi non polari come toluene, benzene e xilene e praticamente insolubile in etere di petrolio.

La sua solubilità può essere influenzata dalla temperatura e dalla presenza di altri soluti. In generale, aumentando la temperatura e la concentrazione del blu di bromotimolo, la sua solubilità in solventi organici può aumentare.
È un acido organico debole nella cui struttura sono contenuti tre anelli benzenici. La sua forma protonata ha un picco di assorbimento a 427 nm e pertanto trasmette la luce gialla. A valori di pH maggiori di 7 si trova in forma deprotonata e ha un picco di assorbimento a 602 nm e trasmette la luce blu. Inoltre, in soluzioni molto acide, ha colore magenta.

La forma protonata e deprotonata sono in equilibrio tra loro. Indicando con HIn la forma protonata e con In– quella deprotonata la reazione di equilibrio è:
HIn ⇄ H+ + In–
Pertanto per il principio di Le Chatelier in ambiente acido l’equilibrio si sposta a sinistra mentre in ambiente basico si sposta a destra.
Preparazione della soluzione di blu di bromotimolo
Stante la sua elevata solubilità in etanolo la soluzione utilizzata per i vari usi è preparata utilizzando l’alcol etilico quale solvente ottenendosi, come spesso accade per gli indicatori acido-base, una soluzione idroalcolica.
Pesare accuratamente 50 mg di blu di bromotimolo in polvere e versarlo in un matraccio tarato da 100,00 mL contenente 4.00 mL di soluzione di idrossido di sodio 0.05 M e 5,00 mL di etanolo al 95% e scaldare su piastra riscaldante. Non utilizzare il becco Bunsen in quanto l’etanolo è infiammabile.
Quando è avvenuta la dissoluzione aggiungere 45.0 mL di etanolo al 95% e diluire a 100 mL con acqua distillata. La concentrazione della soluzione preparata è di circa 0.5 g/L



