Stati allotropici del carbonio: dalla grafite ai nanotubi
Gli stati allotropici del carbonio sono, tra gli altri, carbonio amorfo, grafite, diamante, grafene, nanotubi di carbonio e fullerene
Il carbonio, come alcuni elementi dei Gruppi 13, 14, 15 e 16 della Tavola Periodica mostra diversi stati allotropici. Esso, infatti, può presentarsi in forme diverse che differiscono tra loro per le proprietà fisiche e chimiche oltre che per la forma cristallina pur presentando lo stesso stato di aggregazione.
Stati allotropici del carbonio: diamante
Nel diamante ciascun atomo di carbonio è legato tramite un legame covalente a quattro altri atomi di carbonio contigui tutti ibridati sp3 tramite legami σ.
La struttura del carbonio nel diamante è rappresentata in figura:

Il diamante è un solido rigido, trasparente, elettricamente isolante. E’ la sostanza più dura che si conosca infatti occupa il primo posto nella scala di Mohs.
Tale scala fu ideata nel 1812 dal mineralogista tedesco ed è ancora oggi utilizzata e tiene conto della durezza dei materiali: la scala prende a riferimento dieci materiali che sono ordinati progressivamente secondo la loro durezza dal più tenero caratterizzato dal numero 1 al più duro indicato dal numero più alto, il 10 come si può vedere in figura:

E’ il miglior conduttore di calore: cinque volte maggiore del rame. Queste proprietà ne fanno l’abrasivo ideale, in quanto può scalfire e incidere altre sostanze smaltendo rapidamente il calore generato.
Il diamante è largamente usato in gioielleria e ha prezzi molto diversi a seconda della caratura e della qualità.
Stati allotropici del carbonio: grafite
La grafite è uno dei più comuni stati allotropici del carbonio ed è rinvenuta nelle rocce metamorfiche, ignee e nelle meteoriti.
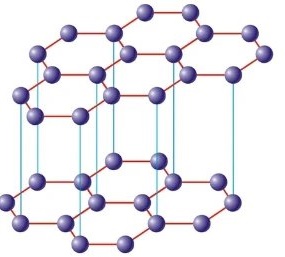
Essa è caratterizzata da una struttura stratificata in cui in ogni strato, gli atomi di carbonio legati tra loro con un legame covalente si trovano in un reticolo cristallino detto a nido d’ape.
Struttura della grafite
Ciascun atomo di carbonio è ibridato sp2 ed è legato, tramite legame covalente, ad altri 3 atomi di carbonio tramite legame σ.
L’elettrone non ibridato appartenente all’orbitale p è delocalizzato. Ciò le conferisce una elevata conducibilità elettrica; la grafite è infatti utilizzata negli elettrodi di grafite.
I vari strati sono legati da deboli legami di van der Waals e pertanto la grafite è un materiale tenero in quanto gli strati possono scorrere l’uno rispetto all’altro, con facilità.
Alla pressione di 1 atm e alla temperatura di 20°C la grafite costituisce la fase termodinamicamente più stabile del carbonio. Tuttavia la velocità di conversione dal diamante alla grafite è del tutto trascurabile. A temperature superiori a 4000 °C il diamante si converte in grafite rapidamente. Per convertire la grafite in diamante occorrono temperature oltre i 1700°C e una pressione di 35 GPa.
A causa della sua elevata stabilità termica e della sua inerzia chimica è utilizzata nei materiali refrattari. Un esempio sono i mattoni refrattari realizzati insieme all’ ossido di magnesio che mostrano:
- alta refrattarietà
- forte resistenza a temperatura elevata
- resistenza alla corrosione
- resistenza alla scheggiatura
Unitamente al biossido di zirconio è usata per refrattari usati nelle acciaierie.
È utilizzata nelle matite di cui costituisce l’anima unitamente all’argilla. Quanto più alto è il contenuto di grafite tanto maggiore è morbida la matita e scura la sua traccia.
Reagisce con il vapore acqueo contenuto nell’atmosfera con formazione di un film sottile che riesce a depositare su qualsiasi superficie riducendone l’attrito ed è quindi usata come lubrificante.
Da essa, può essere ottenuto, tramite esfoliazione meccanica, esfoliazione in fase liquida o tramite metodi chimici il grafene materiale oggetto di intensi studi dalle enormi potenzialità.
Stati allotropici del carbonio: grafene
Il grafene è uno degli stati allotropici del carbonio e il suo spessore corrisponde a quello di un atomo; il carbonio è ibridato sp2 e gli atomi sono disposti secondo un reticolo cristallino a nido d’ape.
Questo materiale ultrasottile è 200 volte più resistente dell’acciaio, flessibilissimo e ottimo conduttore di calore ed elettricità.

Nel 2010 Andre Geim e Konstantin Novoselov dell’Università di Manchester hanno vinto il Premio Nobel per la fisica per i loro studi sul grafene. Già dai primi studi compiuti sul grafene si erano intuite le grandi potenzialità del materiale. Ancora oggi si scoprono ulteriori proprietà che spingono gli scienziati ad approfondire le ricerche al fine di diversi utilizzi.
Difatti, presso il MIT recentemente, sono stati compiuti nuovi esperimenti sorprendenti che hanno mostrato che il grafene assume un comportamento diverso a seconda del materiale con cui è in contatto.
Quando i fogli di grafene, infatti, sono posti su substrati fatti di materiali diversi, alcune proprietà quali:
- la conducibilità elettrica
- l’interazione chimica con altri materiali
si presentano notevolmente diverse a seconda della sostanza che si trova a contatto con il grafene stesso.
Prima che tali studi fossero compiuti ci si aspettava che il grafene esibisse un comportamento simile a quello della grafite.
Si è invece dimostrato come esso, che è prevalentemente usato quale rivestimento di altri materiali di supporto, se a contatto con il biossido di silicio SiO2, materiale largamente usato in elettronica, può rapidamente diventare “attivato” a contatto con determinate sostanze chimiche mentre reagisce con difficoltà con le medesime se il supporto è costituito da nitruro di boro BN.
Proprietà
Il grafene, pertanto, può in essere “attivato” o “disattivato” alla formazione di legami chimici in funzione della sostanza con cui esso si trova a contatto. Tale comportamento è imputabile alla struttura che appare notevolmente influenzata dai campi elettrici degli atomi della sostanza con cui si trova in contatto.
Questa proprietà consente quindi la creazione di dispositivi con un substrato costituito da alcune zone fatte di biossido di silicio e da altre di nitruro di boro ricoperti da grafene il cui comportamento chimico varia in funzione della sostanza che ricopre.
Un tale dispositivo potrebbe consentire, ad esempio, la produzione di microapparati in grado di rilevare tracce di materiali sia chimici che biologici.
Il grafene, inoltre, potrebbe essere usato quale rivestimento protettivo di metalli come il rame in modo da eliminare la tendenza di quest’ultimo ad ossidarsi. Per spiegare il comportamento del grafene si è giunti a un’altra teoria relativa al trasferimento di elettroni. Essa può essere sfruttata per la previsione del comportamento del grafene a contatto con altri materiali.
Un ulteriore passo nell’ambito della ricerca su tale materiale riguarda il comportamento della reattività di un doppio strato di grafene rispetto al singolo strato e, per quanto si sappia, pare che esibisca un comportamento diverso.
Stati allotropici del carbonio: nanotubi di carbonio
I nanotubi di carbonio possono essere considerati, analogamente al fullerene uno degli stati allotropici del carbonio. Il corpo del nanotubo è formato da soli esagoni mentre le strutture di chiusura sono formate da esagoni e pentagoni, esattamente come i fullereni.
La scoperta da parte di Sumio Iijima dei nanotubi di carbonio (CNTs) avvenuta nel 1991 ha inaugurato una nuova era nell’ambito della scienza dei materiali. Lo scienziato giapponese osservò tramite un microscopio elettronico a trasmissione ad altissima risoluzione strutture tubulari di tipo fullerenico nella fuliggine prodotta in una scarica ad arco tra due elettrodi di grafite.

Classificazione
I nanotubi possono essere suddivisi in due tipi:
- nanotubo a parete singola o SWCNT (Single-Walled Carbon NanoTube): costituito da un singolo foglio grafitico avvolto su sé stesso;
- nanotubo a parete multipla o MWCNT (Multi-Walled Carbon NanoTube): formato da più fogli avvolti coassialmente uno sull’altro
Un nanotubo di carbonio a parete singola ha la forma di una cannuccia ed è costituito da un solo strato. I nanotubi di carbonio a parete multipla possono essere costituiti da un minimo di 2 fogli fini a 100 o più fogli che si trovano a una certa distanza e legati da forze interatomiche.
La formazione di un nanotubo a parete singola piuttosto che di un nanotubo a parete multipla dipende dallo stadio più lento del processo di crescita. Se lo stadio più lento è costituito dalla diffusione del carbonio all’interno della particella si avrà crescita preferenziale di MWNT. Invece se la tappa più lenta è l’alimentazione di carbonio alla particella di catalizzatore, si ha formazione preferenziale di SWNT. Il diametro di un SWNT è compreso tra un minimo di 0,7 nm e un massimo di 10 nm. L’elevatissimo rapporto tra lunghezza e diametro dei SWNT consente di considerarli come delle nanostrutture virtualmente monodimensionali, e conferisce a queste molecole delle proprietà peculiari.
Il modo in cui è avvolto il foglio è rappresentato da una coppia di indici (n , m).
I numeri interi n e m indicano il numero di unità di vettori lungo le due direzioni del reticolo cristallino.
Se m = 0, i nanotubi sono detti zigzag, se n = m , i nanotubi sono detti armchair mentre nel caso in cui sono costituiti da esagoni disposti a elica intorno all’asse sono detti chirali.
Le caratteristiche dei nanotubi possono essere diverse a seconda di come il foglio di grafene si è arrotolato per formare il tubo conferendogli caratteristiche di metallo o di semiconduttore.
Queste strutture sono dotate di eccellenti proprietà meccaniche, elettroniche e termiche.
Proprietà
I nanotubi sono tra i materiali più resistenti e duri, hanno bassa densità e proprietà meccaniche come forza tensile e modulo di Young uniche e pertanto costituiscono una risorsa per materiali compositi ad elevata prestazione. La forza e la rigidità dei nanotubi sono dovuti al tipo di legami presenti nella struttura in cui il carbonio è ibridato sp2.
I nanotubi mostrano proprietà di conduttività che cambiano secondo la loro geometria: alcuni mostrano un comportamento metallico, altri comportamento metallico o semiconduttore a seconda dei casi.
Produzione
I nanotubi di carbonio possono essere prodotti sia nei laboratori di ricerca che a livello industriale. Storicamente erano utilizzate due tecniche ovvero la scarica ad arco e l’ablazione laser. Entrambe le tecniche danno luogo alla formazione di nanotubi di carbonio a partire da un bersaglio di grafite in cui vengono inserite piccole quantità di metalli quali ferro, cobalto o nichel.
Il bersaglio è poi bombardato con una sorgente altamente energetica come una scarica elettrica (tecnica della scarica ad arco) o un raggio laser (ablazione laser) che provocano vere e proprie esplosioni nella grafite e quindi la sublimazione del carbonio.
Grazie al metallo contenuto il carbonio sublimato tende ad acquisire una forma cilindrica con ottenimento del nanotubo.
Queste tecniche sono state successivamente abbandonate in quanto la scarica ad arco porta alla formazione di prodotti indesiderati mentre l’ablazione laser comporta l’uso di macchinari eccessivamente costosi.
La tecnica attualmente utilizzata è la deposizione chimica da fase vapore in cui occorrono un substrato solido come il quarzo sul quale avviene la reazione chimica un materiale catalitico come ferro, cobalto o nichel che viene depositato sul substrato e che ha la funzione di iniziatore della reazione e un gas contenente carbonio come metano o acetilene.
Il substrato è riscaldato a una temperatura tra i 600 e gli 800 °C . Quando il gas carbonioso è a contatto con il metallo depositato sul substrato si decompone in carbonio e idrogeno.
Quest’ultimo si disperde nell’atmosfera mentre il carbonio si discioglie nel metallo e, raggiunta la temperatura critica, precipita dando luogo alla formazione del nanotubo.
Usi
L’utilizzo dei nanotubi di carbonio attira un notevole interesse sia da parte del mondo accademico che dall’industria.
Essi possono essere utilizzati in:
- nanoelettronica come diodi e transistori
- supercondensatori
- attuatori elettromeccanici
- sensori chimici
- nelle celle a combustibile
- negli schermi piatti
- impianti biomedici
- dispositivi nanoelettronici
anche se i campi di applicazione appaiono illimitati e ancora oggetto di studi.
Stati allotropici del carbonio: fullereni
I fullereni costituiscono uno degli stati allotropici del carbonio: i due scienziati statunitensi Robert F. Curl e Richard E. Smalley e lo scienziato britannico Harold W. Kroto a cui si deve la scoperta vinsero 1996 il premio Nobel per la Chimica.
Fino ad allora gli unici stati allotropici del carbonio conosciuti erano diamante e grafite. Il nuovo stato allotropico del carbonio grazie alla scoperta di questi scienziati è il fullerene.
Tali strutture unicamente costituite da atomi di carbonio hanno una forma simile a una sfera cava o a un ellissoide che furono denominate buckyball o una forma tubolare denominata buckytube o nanotubi di carbonio.

Nell’ambito della chimica e della scienza dei materiali la struttura più rilevante è quella costituita da 60 atomi di carbonio. A questa specie fu dato il nome di buckminsterfullerene per la somiglianza con le cupole geodetiche progettate dall’architetto Buckminster Fuller la cui struttura fu determinata tramite la spettrometria di massa
Struttura
La struttura con 60 atomi di carbonio è ottenuta vaporizzando barre di grafite in atmosfera di elio. Essa è simile a una sfera cava in cui gli atomi di carbonio sono i vetrici di un icosaedro tronco con 12 pentagoni e 20 esagoni.
Nella struttura proposta ogni vertice dell’icosaedro tronco è occupato da un atomo di carbonio. Ciascuno di essi è legato a tre atomi di carbonio tramite un doppio legame e due legami semplici. Tale struttura suggerisce una ibridazione sp2 ma in tale tipo di ibridazione gli atomi di carbonio giacciono sullo stesso piano come avviene, ad esempio nella grafite.
Nel caso dei fullereni la struttura non è planare e l’angolo tra l’orbitale pz che è di norma perpendicolare al piano diviene di 101.6° introducendo una certa tensione nella molecola
Tuttavia l’alta simmetria fa sì che la tensione sia distribuita uniformemente nella intera struttura con conseguente stabilità della molecola.
Altri stati allotropici del carbonio
La ricerca sul carbonio è ancora in corso per sfruttare al meglio le sue proprietà. Altri stati allotropici del carbonio sono il carbino, il Q-carbon, la nanoschiuma di carbonio, una struttura cristallina porosa con proprietà magnetiche.
Il futuro mostrerà come saranno utilizzate queste e altre strutture. Vi sono buone probabilità che varietà allotropiche di carbonio aiutino a gestire meglio l’energia e migliorare molti processi industriali.
La scoperta di una nuova forma di carbonio
Gli scienziati hanno ottenuto il carbonio poroso ordinato a lungo raggio riscaldando fullereni con nitruro di litio a pressione atmosferica. Il nitruro di litio ha catalizzato la rottura di alcuni dei legami carbonio-carbonio del C60 con formazione di nuovi legami. La preparazione del LOPC apre la strada alla scoperta di altre strutture cristalline a partire dal fullerene. Queste strutture hanno possibili applicazioni nella raccolta, trasformazione e immagazzinamento dell’energia, per generare prodotti chimici e per la separazione di ioni molecolari o gas.



