Sublimazione: aspetti termodinamici
La sublimazione è un passaggio di stato da solido allo stato aeriforme senza passare per lo stato liquido. Tale comportamento, benché non molto comune è tipico, a temperatura ambiente, dello iodio, del naftalene , della canfora e del biossido di carbonio noto come ghiaccio secco.
Come la vaporizzazione anche la sublimazione richiede energia per vincere le forze di attrazione intramolecolari.
La sublimazione può avvenire se un solido ha una pressione di vapore superiore al normale, cioè deve avere deboli attrazioni intermolecolari.
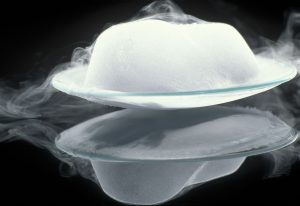
La parola è stata usata dalla fine del 1550 e deriva dal latino sublimatus , che significa “sollevare” ma il processo stesso fu spiegato per la prima volta da Jabir ibn Hayyan latinizzato in Gerber nel 700 che è conosciuto come il più grande alchimista medioevale. Nato in Persia è considerato da molti storici della chimica come un riferimento del passaggio dall’alchimia alla chimica. L’uso più popolare di questo processo è quando il ghiaccio secco passa direttamente dal ghiaccio al vapore
Variazione di entalpia
La variazione di entalpia di sublimazione è l’energia necessaria per convertire una mole di una sostanza dallo stato solido allo stato gassoso.
Ad esempio la variazione di entalpia relativa alla sublimazione del biossido di carbonio relativa al processo:
CO2(s) → CO2(g)
è pari a 26.1 kJ/mol.
La conversione dalla fase solida alla fase liquida richiede una certa energia per superare in parte le forze di attrazione intermolecolari mentre la transizione dallo stato liquido a quello gassoso richiede che tali forze siano completamente superate.
Legge di Hess
Pertanto una descrizione accurata del passaggio di stato solido-gas può essere ottenuta considerando il processo come un processo sequenziale di due fasi secondo la legge di Hess. L’entalpia di sublimazione può essere stimata come la somma delle entalpie di fusione e di vaporizzazione:
solido → liquido ΔHfus
liquido → gas ΔHvap
solido → gas ΔHsub
ΔHsub = ΔHfus + ΔHvap
Tuttavia, in determinate condizioni di pressione e temperatura si può passare direttamente dallo stato solido a quello aeriforme come si può evincere dal diagramma di fase della specie.



