Reazioni di ciclizzazione
Le reazioni di ciclizzazione, dette anche reazioni di anellazione, sono reazioni organiche in cui si ottengono composti ciclici. La formazione di tali composti, che spesso presentano una certa complessità, ne consente l’applicazione in diverse aree nel campo di farmaci e prodotti agrochimici.
Tra le prime reazioni di ciclizzazione vi è la sintesi di Paal-Knorr riportata nel 1884 dai chimici tedeschi Carl Paal e Ludwig Knorr in cui da un 1,4-dichetone e ammoniaca si ottiene un anello pirrolico. Successivamente la reazione è stata adattata anche alla ciclizzazione e dei tiofeni.
Le reazioni di ciclizzazione possono dar luogo alla sintesi di strutture con dimensioni e forme di anelli specifiche, inclusi anelli deformati con elevato controllo stereochimico, caratteristica cruciale nella sintesi di prodotti naturali e nell’industria farmaceutica.
Inoltre le reazioni di ciclizzazione, spesso richiedono meno passaggi e reagenti rispetto ai metodi classici di sintesi, con conseguente minore produzione di rifiuti e riduzione dell’impatto ambientale, in linea con i principi della chimica verde. Negli ultimi decenni, le reazioni di ciclizzazione sono diventate sempre più importanti nella sintesi organica e hanno contribuito allo sviluppo di nuovi composti bioattivi, prodotti agrochimici e polimeri, nonché nuove vie sintetiche per prodotti naturali.
Esempi di reazioni di ciclizzazione
Tra gli esempi più noti di reazioni di ciclizzazione vi è reazione di Diels-Alder è una reazione di addizione coniugata di un diene coniugato a un alchene o alchino (dienofilo) per produrre un cicloesene. Tramite questa reazione si possono unire due scheletri di atomi di carbonio per ottenere un composto ciclico (addotto) per combinazione di due molecole in un processo che coinvolge la conversione di due legami π a due legami σ.

Si dice che tale tipo di reazione è una [4+2] cicloaddizione, in quanto richiede la combinazione di un sistema a 4 elettroni π (il diene) con un sistema a due elettroni π ( l’alchene, chiamato dienofilo). La reazione risulta inoltre termodinamicamente favorita a causa della conversione di due legami π in due nuovi legami σ forti.
Un classico esempio di reazione di Diels-Alder è quello che avviene tra il 2-metil-1,3-butadiene e l’anidride maleica che dà, come prodotto di reazione con una resa intorno al 97% l’anidride 4-metil-1,2,3,6-tetraidroftalica.

Un altro tra gli esempi di reazioni di ciclizzazione vi è la ciclizzazione di Nazarov che prevede l’attivazione del chetone con ottenimento di un catione pentadienilico che dà luogo alla ciclizzazione. La reazione prevede l’attivazione di un divinilchetone con un acido di Lewis: lo stadio caratterizzante la reazione coinvolge la chiusura di un anello tramite una reazione elettrociclica ovvero un riarrangiamento periciclico in cui un legame π viene trasformato in un legame σ o viceversa.
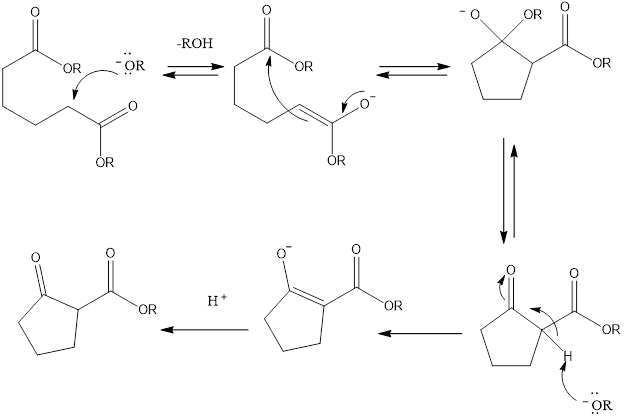
Un altro esempio è fornito dalla condensazione di Dieckmann dal nome del chimico tedesco Walter Dieckmann, condensazione intramolecolare catalizzata da basi di un diestere che dà, come prodotto di reazione, un β-chetoestere ciclico abitualmente costituito da cinque o sei atomi di carbonio.
Il meccanismo appare di particolare importanza poiché incorpora molte delle proprietà reattive chiave degli esteri: deprotonazione per dare enolati, azione degli enolati quali nucleofili e reazione di addizione-eliminazione ovvero sostituzione nucleofila acilica dell’estere.
Ciclizzazione radicalica
Le reazioni di ciclizzazione radicaliche, che avvengono secondo un meccanismo radicalico, sono utilizzate per la sintesi sia di anelli carbociclici che eterociclici che sistemi mono e policiclici. In generale, le reazioni di ciclizzazione radicalica comprendono tre fasi fondamentali: generazione selettiva di radicali, ciclizzazione radicalica e conversione del radicale ciclizzato nel prodotto.
Le ciclizzazioni radicaliche sono reazioni essenziali nella biosintesi dei metaboliti secondari e nella sintesi chimica di molecole. In natura vi sono enzimi atti a catalizzare queste trasformazioni per la sintesi di prodotti naturali strutturalmente complessi. I biocatalizzatori in grado di catalizzare queste reazioni di ciclizzazione radicaliche ovvero la monoossigenasi del citocromo P450, la diossigenasi ferro non eme e α-chetoglutarato-dipendenti e il radicale S -adenosilmetionina (SAM).
Le reazioni radicaliche di trasferimento atomico sono trasformazioni chimiche che non si verificano naturalmente nei sistemi biologici. Tuttavia, i metalloenzimi possono catalizzare tali reazioni aprendo così la strada a percorsi biocatalitici verso le polimerizzazioni radicaliche a trasferimento atomico e le ciclizzazioni radicaliche a trasferimento atomico



