Reattivo di Brady: sintesi, reazioni
La 2,4-dinitrofenilidrazina è meglio conosciuta come reattivo di Brady dal chimico statunitense St Elmo Brady è usata nella caratterizzazione del gruppo carbonilico di aldeidi e chetoni.
Il reattivo di Brady ha formula (NO2)2C6H5NHNH2 e struttura:
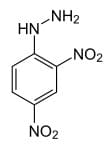
E’ una sostanza scarsamente solubile in acqua che si presenta allo stato solido di colore rosso-arancio sensibile agli urti. E’ infiammabile e potenzialmente esplosiva pertanto se ne consiglia l’uso solo quando viene preventivamente bagnata.
Sintesi del reattivo di Brady
E’ sintetizzato a partire dal 2,4-dinitroclorobenzene e dal solfato di idrazina in presenza di acetato di potassio secondo la reazione
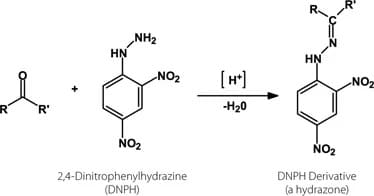
Il solfato di idrazina (N2H6)SO4 è il sale dell’idrazina e dell’acido solforico .L’idrazina infatti è un composto basico che in presenza di acido solforico dà luogo al sale noto anche come solfato di idrazonio.
Per preparare il reattivo di Brady si mettono in un becker da 400 mL 35 g di solfato di idrazina in 125 mL di acqua calda e aggiungere, mescolando, 85 g di acetato di potassio. La soluzione è fatta bollire per 5 minuti e poi raffreddata a circa 70°C. Sono aggiunti 75 mL di etanolo e il precipitato formatosi viene filtrato per suzione e lavato con alcol caldo.
La soluzione di idrazina filtrata è utilizzata successivamente.
In un pallone da 1 L cui è collegato un refrigerante a ricadere sono posti 50.5 g di 2,4-dinitroclorobenzene disciolti in 250 mL di etanolo. E aggiunta la soluzione di idrazina e la miscela è scaldata a riflusso sotto agitazione per circa un’ora.
Dopo raffreddamento si opera una filtrazione e si lava il precipitato di colore rosso con 50 mL di alcol a 60°C per rimuovere l’alogenuro che non ha reagito e successivamente con 50 mL di acqua calda.
Reazioni
Il reattivo di Brady reagisce rapidamente con il gruppo carbonilico di aldeidi e chetoni tramite una reazione di condensazione. Il doppietto elettronico solitario presente sull’azoto del gruppo –NH2 lo rende un forte nucleofilo. La reazione avviene per attacco nucleofilo della 2,4-dinitrofenilidrazina al carbonio carbonilico per dare un precipitato costituito da idrazone.
Se il composto contenente il gruppo carbonilico è alifatico il precipitato è di colore giallo mentre se è aromatico il precipitato è rosso.
La reazione è descritta come una reazione di condensazione in quanto due molecole si combinano tra loro per dare una molecola con un maggior peso molecolare ed eliminazione di una molecola di acqua. Tale reazione può, tuttavia, essere considerata come una reazione di addizione-eliminazione in quanto avviene l’addizione nucleofila del gruppo –NH2 al carbonio carbonilico seguita dall’allontanamento di una molecola di acqua.




