Nitrosazione: esempi, applicazioni
La nitrosazione è una reazione in cui il gruppo NO è introdotto in una molecola organica.
Quando è legato in modo covalente a un atomo di carbonio, azoto, ossigeno o zolfo, il gruppo NO è indicato come gruppo nitroso. Se è coordinato a un metallo di transizione, è indicato come gruppo nitrosile.
In condizioni fisiologiche, le reazioni di nitrosazione portano alla formazione di tre tipi di legami X-NO:
- S- nitroso come quello della S- nitrosocisteina
- N- nitroso come quello nell’ N- nitrosotriptofano
- complessi ferro-nitrosile
Storia
Le reazioni di nitrosazione sono note da oltre 150 anni. I primi lavori riguardavano le reazioni delle ammine. Sembra che il chimico italiano Raffaele Piria abbia condotto per la prima volta le reazioni con ammine primarie alifatiche nel 1846. Successivamente il chimico tedesco August Wilhelm von Hofmann chimico tedesco Hofmann lavorò con ammine aromatiche primarie. Johann Peter Griess iniziò il lavoro sulla chimica dei sali di diazonio e caratterizzò le nitrosammine
Victor Meyer dimostrò nel 1873 che la nitrosazione al carbonio era possibile quando isolò gli acidi nitrolici caratterizzati dal gruppo funzionale RC(NO2)=NOH da nitrocomposti
Ulteriori studi sulla nitrosazione hanno portato all’utilizzo di queste reazioni su scala industriale. L’idrossilammina è prodotta dal processo Raschig che comporta la nitrosazione del bisolfito. Quella dei derivati del cicloesano porta all’ε-caprolattame da cui si ottiene il nylon.
Inoltre i nitrosocomposti sono utilizzati nell’industria della gomma.
Reazioni di nitrosazione
Affinché si abbia una nitrosazione si deve ottenere lo ione nitrosonio NO+ detto anche nitrosile.
Lo ione nitrosonio è generato in situ facendo reagire un nitrito come quello di sodio in ambiente acido. Si forma così l’acido nitroso che è ulteriormente protonato. La perdita di una molecola di acqua porta alla formazione del catione poliatomico che è stabilizzato per risonanza:
Esempi
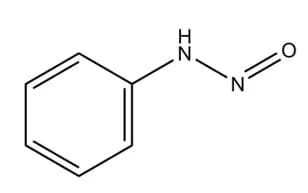
Un esempio è quello dell’anilina in cui il doppietto elettronico solitario dell’azoto attacca lo ione nitrosonio. Si ottiene un intermedio in cui l’azoto dell’anilina ha una carica positiva. A seguito della sua deprotonazione si ottiene la N-fenil-nitrosammina
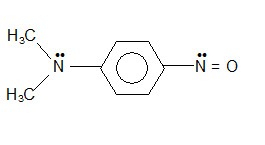
La nitrosazione della N,N-dimetilanilina porta alla formazione della p-nitroso- N,N-dimetilanilina
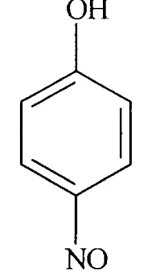
Per nitrosazione del fenolo si ottiene il p-nitrosofenolo