Litio diisopropilammide: sintesi, reazioni, prodotto cinetico e termodinamico
Il litio diisopropilammide noto come LDA è una base forte avente formula [(CH3)2CH]2NLi solubile in solventi non polari.
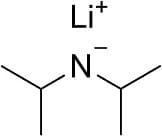
È usato nell’ambito delle sintesi organiche per deprotonare gli acidi deboli. Stante la sua struttura, dotata di ingombro sterico intorno all’atomo di azoto, è un debole nucleofilo pertanto viene adoperato per evitare reazioni indesiderate.
Sintesi del litio diisopropilammide
È ottenuto solubilizzando la diisopropilammina in tetraidrofurano e trattando la soluzione con n-butillitio secondo la reazione acido base con una costante di equilibrio dell’ordine di 1015:
[(CH3)2CH]2NH + CH3(CH2)3Li → [(CH3)2CH]2NLi + CH3(CH2)2CH3
Il litio diisopropilammide, per la sua basicità, è utilizzato in particolare per spostare a destra l’equilibrio tra chetone e enolato.
Infatti facendo reagire un chetone con α-idrogeni con una base forte come NaOH esso risulterà solo parzialmente enolizzato mentre se è fatto reagire con LDA il prodotto è costituito essenzialmente da enolo.
Reazioni
Nelle reazioni di enolizzazione il litio diisopropilammide agisce selettivamente nella rimozione del protone: ad esempio nel caso di un chetone come il 3-metil, butan-2-one, l’LDA rimuove l’idrogeno dal carbonio meno sostituito ovvero che ha il maggior numero di atomi di idrogeno:
Un esempio è costituito dal 2-metilcicloesanone:

Esso presenta due atomi di carbonio in α al carbonile. Uno è legato a due atomi di idrogeno e l’altro è legato ad uno solo. Si possono ottenere due prodotti di reazione a seconda dell’idrogeno che viene allontanato dalla base.
Questo tipo di reazione è regolato da un fattore cinetico e da un fattore termodinamico infatti riportando in grafico l’energia in funzione della coordinata di reazione si formano due intermedi. Uno dei due ha un’energia di attivazione minore e si forma più velocemente e il prodotto è detto prodotto cinetico.
L’altro intermedio ha un’energia cinetica maggiore quindi si forma più lentamente e il prodotto, detto prodotto termodinamico ha una maggiore stabilità
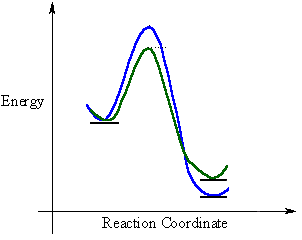
Quando il 2-metilcicloesanone è trattato in ambiente basico si può ottenere il prodotto A che è il prodotto cinetico in quanto l’allontanamento del protone meno impedito avviene in modo più rapido mentre il prodotto B è quello termodinamico che ha una maggiore stabilità in quanto l’enolato formatosi presenta un doppio legame più sostituito.
Nel caso della reazione del 2-metilcicloesanone con una base si possono quindi ottenere sia il prodotto A che il prodotto B.
Il prodotto A costituisce quello ottenuto secondo il controllo cinetico in quanto la base estrae più rapidamente l’idrogeno meno impedito. Il prodotto B invece è quello ottenuto secondo il controllo termodinamico che è il più stabile.
In presenza di una base debole come la trietilammina si ottiene circa l’80% di composto B. Infatti il prodotto derivante dall’allontanamento dell’idrogeno meno impedito è in equilibrio con il reagente. Esso è a sua volta può lentamente essere deprotonato portando al prodotto più stabile.
Viceversa l’utilizzo del litio diisopropilammide porta alla formazione del 99% di prodotto A e dell’ 1% di prodotto B. Infatti essendo una base forte ed impedita stericamente, riesce ad allontanare con più facilità l’idrogeno meno impedito.






