Addizione radicalica di HBr ad un alchene
L’addizione radicalica di HBr ad un alchene avviene con orientazione anti-Markovnikov e infatti nel caso del propene si ottiene l’1-bromo,2-metilpropano
Molte reazioni di addizione agli alcheni possono essere catalizzate da piccole quantità di perossidi, o di azocomposti termolabili o per irradiazione con luce ultravioletta. Le reazioni che hanno luogo sotto queste condizioni sono, quasi senza eccezioni, reazioni a catena di radicali liberi.
Reazione a catena
Consideriamo, ad esempio, l’addizione di HBr al propene:
Iniziazione:
C6H5COOCOC6H5 (dibenzoilperossido) → 2 C6H5CO2· (radicale benzoilossi)
C6H5CO2· + HBr → C6H5COOH + Br·
Propagazione:
Br· + CH2CH=CH2 → CH3C·HCH2Br
CH3C·HCH2Br + HBr → CH3CH2CH2Br + Br·
Terminazione:
2 Br· → Br2
CH3C·HCH2Br + Br· → CH3CHBrCH2Br
2 CH3C·HCH2Br → Br-CH2CH(CH3)-CH(CH3)CH2Br
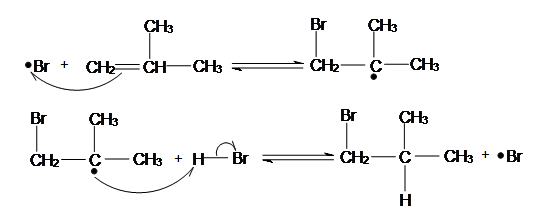
Tale reazione porta ad un prodotto anti-Markovnikov pertanto si possono ottenere dagli alcheni alogenuri alchilici che hanno l’alogeno sull’atomo di carbonio che ha più idrogeni. L’addizione di HBr ad un alchene per via radicalica costituisce un metodo per la preparazione di bromuri primari anche se di regola viene preferita l’idroborazione. Il meccanismo di addizione radicalica è mostrato in figura:
L’addizione radicalica di Br· al 2-metil-1-propene avviene sul primo carbonio in quanto si forma, come intermedio, il radicale più stabile. Si ricordi che la stabilità relativa dei radicali segue l’ordine:
terziario > secondario > primario
L’orientazione nella addizione radicalica ad un doppio legame è la stessa che nell’addizione di un protone pertanto i prodotti finali di addizione di HBr nella reazione ionica che avviene per formazione di un carbocatione e nella reazione radicalica sono diversi perché in un caso l’idrogeno entra per primo dando luogo alla formazione del carbocatione più stabile mentre nell’altro caso è il bromo ad entrare per primo dando luogo alla formazione del radicale più stabile.
Poiché le reazioni di propagazione della catena si ripetono continuamente la decomposizione di una singola molecola di iniziatore può produrre un gran numero di molecole del prodotto. La reazione ha termine quando due trasportatori della catena (due radicali liberi) si incontrano.
La reazione di addizione radicalica di HCl e HI non avviene. Nel primo caso, infatti, il legame idrogeno-cloro è troppo forte per essere spezzato nelle condizioni di esercizio. Nel secondo caso, invece, se da un lato il legame idrogeno- iodio si rompe con facilità, il radicale iodio non si addiziona altrettanto rapidamente agli alcheni.