Spettroscopia UV/Visibile: applicazioni, cromofori
La spettroscopia UV/Visibile è usata per la determinazione di molti analiti tra cui ioni di metalli, composti coniugati e macromolecole biologiche. Si applica a metalli di transizione, composti coniugati e macromolecole biologiche.
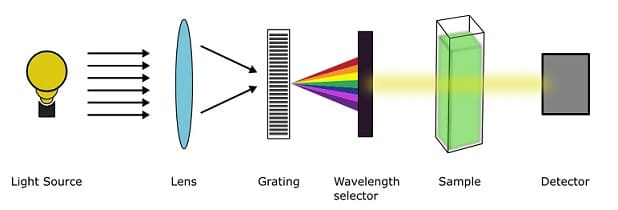
La spettroscopia UV/Visibile è una tecnica utilizzata per eseguire analisi sia qualitative che quantitative di un campione utilizzando una sorgente di luce nell’intervallo di lunghezze d’onda ultraviolette di 200–400 nm fino all’intervallo di lunghezze d’onda visibili di 400–700 nm.
L’interazione tra la sorgente luminosa e il campione può essere analizzata attraverso l’assorbimento, la trasmissione o la riflessione nello spettro UV-Vis. Il picco caratteristico nello spettro UV-Vis è una rappresentazione del legame energetico del campione. L’esistenza di coniugazione e delocalizzazione influenza in modo significativo la lunghezza d’onda dei picchi caratteristici nello spettro UV-Vis.
Applicazioni della spettroscopia UV/Visibile
Tra le tante applicazioni della spettroscopia UV/Visibile vi sono:
Rilevamento di impurezze
La spettroscopia di assorbimento UV/Visibile è uno dei metodi migliori per la determinazione di impurezze presenti nelle molecole organiche. In particolare si può controllare la purezza di solventi esaminando quella regione dello spettro in cui essi dovrebbero essere completamente trasparenti.
Per esempio le impurezze di solfuro di carbonio in tetracloruro di carbonio danno un assorbimento a 318 nm, mentre quelle di benzene in cicloesano danno un assorbimento a 255 nm. L’identificazione di un prodotto naturale o di sintesi particolarmente complesso può essere fatta mediante confronto del suo spettro con quello del prodotto naturale.
Ricerca dei cromofori
Nell’analisi di uno spettro si devono tenere conto alcune regole fisse. Se lo spettro è relativamente semplice e le bande si trovano completamente nella regione 200-350 nm si può pensare alla presenza di un cromoforo organico semplice, al massimo coniugato con un altro cromoforo semplice o con un gruppo auxocromo.
Se lo spettro è composto da molte bande che arrivano fino al visibile allora si tratta di un cromoforo organico esteso e molto coniugato oppure di un composto dei metalli di transizione dei lantanidi.
Bisogna poi valutare l’intensità delle bande. Tuttavia in uno spettro molto complesso alcune bande che dovrebbero essere relativamente deboli possono risultare intense perché si sovrappongono ad altre bande.
Una volta caratterizzati qualitativamente i cromofori da cui hanno origine gli assorbimenti si può far uso:
- della regola di Woodward
- paragonando lo spettro ottenuto con quello già noto di molecole che hanno un sistema elettronico simile a quello ipotizzato dopo la prima analisi dello spettro.
I dati negativi di uno spettro UV/Vis possono fornire utili indicazioni. Ad esempio se un composto non assorbe sopra i 200 nm esso è quasi certamente un composto saturo
Analisi quantitativa
Una delle maggiori applicazioni della spettroscopia UV/Visibile è la determinazione quantitativa di un analita tramite la legge di Lambert-Beer dovuta a Johann Heinrich Lambert e August Beer.

Secondo la legge vi è una relazione lineare tra la concentrazione e la densità ottica misurata a una definita lunghezza d’onda generalmente sfruttata mediante una retta di taratura. La legge di Lanbert-Beer è generalmente soddisfatta nella spettroscopia UV/Vis in un largo campo di concentrazioni
Determinazione della velocità di una reazione
La velocità di una reazione può essere determinata tramite la spettroscopia UV/Visibile misurando in quanto tempo uno dei reagenti o uno dei prodotti delle reazione assorbe la luce UV o visibile a una lunghezza d’onda per la quale le altre specie (reagenti e prodotti) mostrano una assorbanza nulla o di lieve entità.
Ad esempio, in soluzione basica il nitroetano CH3CH2NO2 si trasforma nell’anione nitroetano CH3C–HNO2 con formazione di acqua. L’anione mostra una λmax a 240 nm e né l’acqua, né il nitroetano danno un’assorbanza significativa a tale lunghezza d’onda. Per misurare la velocità alla quale lo ione OH– strappa un protone dal nitroetano ovvero la velocità alla quale si forma l’anione del nitroetano, si misura l’assorbanza a 240 nm in funzione del tempo.



