Fosfomolibdato di ammonio: sintesi, usi
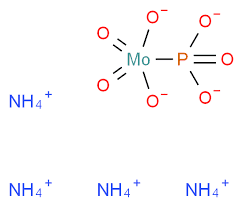
Il fosfomolibdato di ammonio (YAPM) è un sale inorganico avente formula (NH4)3PMo12O40 in cui il molibdeno ha numero di ossidazione + 6 e il fosforo +5. Nella specie il molibdeno presenta il numero di ossidazione più alto
Si presenta sotto forma di cristalli di colore giallo poco solubili in acqua. Il fosfomolibdato si ammonio appartiene alla categoria dei poliossometallati (POM). Il fosfomolibdato di ammonio è stato il primo poliossometallato scoperto quasi due secoli fa da Berzelius e veniva utilizzato come agente riducente
Sintesi del fosfomolibdato di ammonio
Esso è ottenuto dalla reazione tra acido fosforico e ortomolibdato di ammonio in presenza di un eccesso di acido nitrico:
H3PO4 + 12 (NH4)2MoO4 + 21 HNO3 → (NH4)3PMo12O40 + 21 NH4NO3 + 12 H2O
Dalla reazione si ottiene anche il nitrato di ammonio che è solubile in acqua.
La formazione del fosfomolibdato di ammonio è evidenziata dalla formazione del precipitato di colore giallo canarino. Il fosfomolibdato di ammonio verde (GAPM) è ottenuto dallo YAPM dopo irradiazione UV ( λ ≈ 365 nm) per 6 ore.
Determinazione dei fosfati
La determinazione del fosfato inorganico è fatta tramite la reazione con il molibdato di ammonio. Dalla reazione tra il fosfato e il molibdato di ammonio si ottiene il fosfomolibdato di ammonio.
Il fosfomolibdato di ammonio è ridotto da un riducente come l’N-metil-p-amminofenolo solfato o l’acido 1-ammino-2-naftolo-4-solfonico H2NC10H5(OH)SO3H. Si ottiene un complesso blu che denota la presenza di fosfato
Usi
Il fosfomolibdato di ammonio è utilizzato per preparare catalizzatori supportati da alluminosilicati. Essi trovano applicazione nella disidratazione del glicerolo in fase gassosa con ottenimento dell’acroleina secondo la reazione:
CH2OHCHOHCH2OH → CH2=CH-CH=O + 2 H2O
Particelle microdimensionate sono in grado di rimuovere coloranti cationici dalle acque. Questo comportamento è attribuito allo scambio ionico tra gli ioni ammonio con frazioni coloranti cationici.
È inoltre utilizzato come scambiatore di ioni inorganici per l’eliminazione di alcuni ioni dai rifiuti liquidi. ha dimostrato di essere un adsorbente efficiente per applicazioni ambientali come scambiatore di cationi. In forma microporosa è utilizzato quale catalizzatore per utilizzato per degradare gli antibiotici tetraciclinici in condizioni ambientali.
Questa azione catalitica è dovuta al fatto che il molibdeno con numero di ossidazione + 6 passa a numero di ossidazione + 5 e quest’ultimo durante il processo viene ossidato nuovamente a numero di ossidazione + 6.
Grazie a questa caratteristica i poliossometallati e, in particolare il fosfomolibdato di ammonio, sono usati nell’industria della raffinazione e per la produzione di sostanze chimiche fini, per l’ossidazione dell’isobutano ad acido metacrilico, per l’idratazione delle olefine come il butadiene, nella trasformazione di metanolo in idrocarburi, desolforazione del diesel e per la fotodegradazione dei coloranti



