Valutazione quantitativa degli amminoacidi con ninidrina, reazioni
La valutazione quantitativa degli amminoacidi può essere fatta ricorrendo a diversi tipi di test come quello con la ninidrina e quello xantoproteico
Gli α-ammonoacidi sono i monomeri di cui è costituita una proteina; gli α-amminoacidi che si trovano nelle proteine sono 20 e sono costituiti da un gruppo carbossilico –COOH e da un gruppo amminico –NH2 legati allo stesso atomo di carbonio:
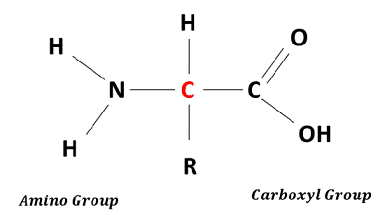
Gli amminoacidi presentano dimensioni, carica elettrica e solubilità in acqua diverse a causa della presenza della carena laterale R che varia a seconda dell’amminoacido.
Di fondamentale importanza nello studio delle proteine è l’individuazione e la valutazione quantitativa degli amminoacidi presenti.
Analisi quantitativa
Un metodo per la valutazione quantitativa degli amminoacidi presenti in una proteina è quello che utilizza la ninidrina.
La ninidrina è un solido giallo dall’odore tenue caratteristico:

Reazioni per la valutazione quantitativa degli amminoacidi
Gli α-amminoacidi reagiscono con la ninidrina e si verifica una variazione di colore secondo i seguenti stadi:
1) α-amminoacido + ninidrina → α-imminoacido + forma ridotta della ninidrina + 2 H2O
Tale stadio è una deaminazione ossidativa che porta all’allontanamento di due idrogeni dall’ α-amminoacido con ottenimento di un α-imminoacido; la ninidrina si trasforma nella sua forma ridotta perdendo un ossigeno.
2) α-imminoacido + H2O → α-chetoacido + NH3
La rapida idrolisi del gruppo –NH nell’ α-imminoacido porta alla formazione di un α-chetoacido che partecipa successivamente alla reazione di decarbossilazione
3) α-chetoacido + NH3 → aldeide + CO2
In tale reazione l’aldeide formata ha un atomo di carbonio in meno rispetto all’amminoacido di partenza. Da queste reazioni si ottengono i reagenti necessari ad ottenere il prodotto finale che si presenta di colore blu-viola.
La reazione complessiva può essere schematizzata come segue:
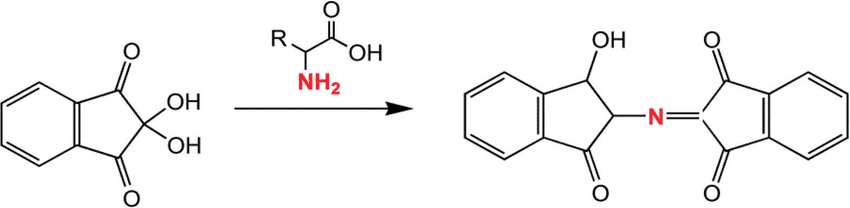
L’intensità del colore è direttamente proporzionale alla concentrazione dell’amminoacido pertanto si può condurre un’analisi colorimetrica e, tramite la legge di Lambert-Beer si può ottenere la concentrazione degli amminoacidi presenti.
Nella valutazione quantitativa degli amminoacidi con ninidrina l’assorbanza del complesso ottenuto, detto porpora di Ruhemann è a 570 nm.



