Penicillina: struttura, tipi
La penicillina è il primo antibiotico ottenuto nel 1927 da Alexander Fleming utilizzata nel trattamento di molte infezioni di origine batterica. Per la sintesi si utilizza una fermentazione che comprende la fermentazione vera e propria, l’uso di prodotti chimici quali precursori, i microrganismi, il substrato nutriente, la sterilizzazione e l’apparecchiatura industriale di produzione dell’antibiotico.
Le penicilline appartengono alla famiglia dei metaboliti microbici chiamati comunemente antibiotici. Tutte le penicilline possiedono struttura molto simile e hanno, come caratteristica comune, l’ azione battericida verso i batteri Gram-positivi.
Struttura della penicillina
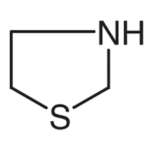
Il nucleo fondamentale della molecola è un sistema biciclico contenente un anello β- lattamico fuso con un anello tiazolidinico. L’anello β-lattamico a quattro membri è un lattame ovvero una un’ammide ciclica. La tiazolidina è un composto organico eterociclico con la formula (CH2)3(NH)S. È un anello saturo a 5 membri con un gruppo tioetere e un gruppo amminico nelle posizioni 1 e 3.
Le varie penicilline commerciali differiscono tra loro unicamente per i gruppi costituenti la catena laterale unita al sistema biciclico. Tutti gli antibiotici contenenti la struttura β- lattamica esercitano il loro effetto biologico per specifica inibizione della sintesi di certi componenti essenziali delle pareti delle cellule batteriche. Le cellule dei Mammiferi, non avendo costituenti analoghi, non sono sostanzialmente influenzate dalle penicilline. Delle sei penicilline naturali note, solo una ha trovato applicazione come agente antinfettivo ed è la penicillina G o benzil-penicillina.
A questa molecola, di prima generazione, è seguita una serie di penicilline di seconda generazione o biosintetiche ottenute per addizione di precursori, come l’acido fenilacetico, nel caso della benzil-penicillina al liquido di fermentazione. Tale aggiunta

aumenta la resa del prodotto specifico e riduce il contenuto di altri derivati meno attivi nel prodotto di fermentazione. Fra i più importanti prodotti biosintetici vi è la fenossimetilpenicillina ( penicillina V) ottenuta per addizione di acido fenossimetilacetico o fenossietanolo al liquido di fermentazione.
Questa specie sintetica, a differenza di quelle naturali, ha il vantaggio di essere abbastanza resistente agli acidi diluiti e non è quindi distrutta dai succhi gastrici quindi può essere somministrata per via orale.
Penicilline semisintetiche
La terza generazione, quella delle penicilline semisintetiche, è ottenuta dai liquidi di fermentazione a cui non sia stato aggiunto acido feniacetico o altro precursore. Da essi può essere isolato il componente base delle penicilline, l’acido 6-aminopenicillanico.
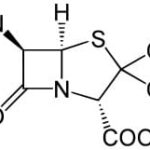
Questo prodotto, la cui struttura è stata identificata nel 1961 può essere facilmente acilato e molti dei suoi derivati così ottenuti sono stabili, oltre che verso gli acidi, anche verso l’enzima penicillinasi. Tale enzima, che viene prodotto da certi batteri, distrugge la maggior parte delle penicilline per scissione idrolitica dell’anello del β-lattame. La scoperta delle penicilline semisintetiche ha reso possibile trattare le infezioni causate da batteri che producono questo enzima e che sono quindi penicillino-resistenti.
Le penicilline hanno tutte la struttura fondamentale dell’acido 6-amminopenicillanico che, secondo la nomenclatura ufficiale è indicato come acido 6-ammino-3,3-dimetil-7oxo-4-tia-1-azabiciclo[3,2,0]-eptan-2-carbossilico:

Tutte le penicilline note sono degli acilderivati dell’acido 6-amminopenicillanico e si differenziano tra loro per la natura del gruppo acilico R-CO- unito all’amminogruppo.
Tabella
Alcuni tipi di penicilline, con i rispettivi nomi commerciali, noti nella farmacopea ufficiale e la struttura della catena laterale R-CO-
Nome commerciale | Denominazione chimica | Catena laterale R |
Naturali: | ||
F | 2-pentenilpenicillina | CH3-CH2-CH=CH-CH2– |
G | benzilpenicillina | C6H5-CH2– |
Biosintetiche: | ||
V | fenossimetilpenicillina | C6H5-O-CH2– |
O | allilmercaptometilpenicillina | CH2=CH-CH2-S-CH2– |
Semisintetiche: | ||
Feneticillina | fenossietilpenicillina | C6H5-O-CH(CH3)- |
Fenbenicillina | fenossimetilpenicillina | C6H5-O-CH-(C6H5)- |
Le penicilline sono relativamente stabili a pH compresi tra 5 e 8. Al di fuori di questo intervallo si degradano, ed è questo uno dei morivi che inizialmente hanno reso infruttuosi molti tentativi di sintesi e di caratterizzazione.
Con alcali acquosi si idrolizzano facilmente e, per successiva acidificazione, danno acidi penicilloici.



