Metodi per distinguere aldeidi e chetoni
Tra i metodi per distinguere aldeidi e chetoni vi è quello di sottoporre il composto a ossidazione in presenza di ossidanti come bicromato di potassio
In condizioni acide, infatti, le aldeidi sono ossidate ad acidi carbossilici mentre in condizioni basiche il prodotto di reazione è il sale dell’acido carbossilico:
RCOH → RCOOH ( condizioni acide)
RCOH → RCOO– ( condizioni basiche)
Nel caso della formaldeide (metanale) HCOH l’ossidazione porta alla formazione di biossido di carbonio e acqua; l’acido formico (acido metanoico) o lo ione formiato (metanoato) che si formano dall’ossidazione, infatti, sono ulteriormente ossidati.
Le semireazione di ossidazione di una aldeide è la seguente:
In condizioni acide: RCHO + H2O → RCOOH + 2 H+ + 2 e–
In condizioni basiche: RCHO + 3 OH– → RCOO– + 2 H2O + 2 e–
Sono mescolate una piccola quantità di bicromato di potassio in soluzione acidificata con acido solforico diluito e qualche goccia di aldeide o chetone. Se la reazione non avviene a freddo, si può scaldare dolcemente a bagnomaria per qualche minuto. Nel caso sia stata aggiunta un’aldeide la soluzione vira dal colore arancio a quello verde. La semireazione di riduzione dello ione bicromato è:
Cr2O72- + 14 H+ + 6 e– → 2 Cr3+ + 7 H2O
La semireazione di ossidazione di un’aldeide è:
RCHO + H2O → RCOOH + 2 H+ + 2 e –
La reazione complessiva diviene pertanto:
3 RCHO + Cr2O72- + 8 H+ → 3 RCOOH + 2 Cr3+ + 4 H2O
I chetoni, al contrario, resistono all’ossidazione e solo agenti fortemente ossidanti quale lo ione permanganato portano ad un’ossidazione che porta alla demolizione della molecola con rottura dei legami carbonio-carbonio. Trattando un chetone con bicromato di potassio non avviene alcuna reazione e, se trattati con una soluzione di bicromato di potassio acidificata con acido solforico il colore della soluzione non varia a riprova che non è avvenuta alcuna ossidazione
Saggio di Tollens
Il reattivo di Tollens è preparato facendo reagire nitrato di argentoAgNO3 con idrossido di sodio NaOH con formazione di ossido di argento secondo la reazione:
2 AgNO3 + 2 NaOH → 2 NaNO3 + Ag2O + H2O
L’ossido di argento è solubilizzato con aggiunta di ammoniaca in eccesso con formazione dello ione diamminoargento [Ag(NH3)2]+ secondo la reazione:
Ag2O + 4 NH3 + H2O → 2 [Ag(NH3)2]+ + 2 OH–
Le aldeidi riducono lo ione diamminoargento ad argento metallico e, stante l’ambiente basico della soluzione, le aldeidi si ossidano al sale dell’acido carbossilico.
La semireazione di riduzione dello ione diamminoargento è:
[Ag(NH3)2]+ + 1 e– → Ag + 2 NH3
La semireazione di ossidazione di un’aldeide in condizioni basiche è:
RCHO + 3 OH–→ RCOO– + 2 H2O + 2 e–
La reazione che avviene complessivamente è:
2 [Ag(NH3)2]+ + RCHO + 3 OH–→ RCOO– + 2 Ag + 4 NH3 + 2 H2O
Dalla soluzione incolore si ottiene un precipitato grigio di argento metallico.
I chetoni non reagiscono con il reattivo di Tollens.
Saggio di Fehling o saggio di Benedict
Entrambi i saggi sono effettuati con soluzioni contenente complessi del rame (II) in soluzione basica. In entrambi i saggi il reattivo ossidante è lo ione Cu2+ che ossida le aldeidi ma non i chetoni.
La soluzione di Fehling dovuta al chimico tedesco Hermann von Fehling è preparata mescolando una soluzione di solfato di rame (II) e una soluzione di tartrato di sodio e potassio in ambiente basico per NaOH. Gli ioni tartrato complessano gli ioni rameici impedendone la precipitazione come idrossido di rame (II).
La soluzione di Benedict contiene ioni rame (II) complessati con ioni citrato in una soluzione di carbonato di sodio. La complessazione dello ione rame (II) ne impedisce la precipitazione come carbonato di rame (II).
La semireazione di riduzione dello ione rame (II) sia nella soluzione di Fehling che in quella di Benedict è la seguente:
2 Cu2+ + 2 OH- + 2 e– → Cu2O + H2O
La semireazione di ossidazione delle aldeidi è:
RCHO + 3 OH–→ RCOO– + 2 H2O + 2 e–
E quindi la reazione complessiva risulta:
RCHO + 5 OH– + 2 Cu2+→ RCOO– + 3 H2O + Cu2O
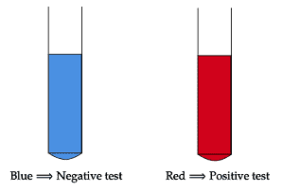
La soluzione del reattivo di Benedict è caratterizzata da una intensa colorazione blu; in presenza di un’aldeide si forma un precipitato rosso mattone di ossido di rame (I)



