Alcani: reazioni
Gli alcani danno poche reazioni in quanto essi sono composti che hanno scarsa affinità chimica con altre sostanze. Essi sono denominati paraffine dal latino parum affinis ovvero poco affine che in senso lato significa poco inclini alle reazioni
Gli alcani sono composti organici saturi in cui il carbonio è ibridato sp3 e hanno formula generale CnH2n+2.
Poiché sono presenti solo legami forti di tipo σ, gli alcani, contrariamente agli alcheni e agli alchini, sono piuttosto stabili e danno luogo a un numero limitato di reazioni.
Reazioni degli alcani
Le reazioni tipiche degli alcani sono: combustione, alogenazione e cracking.
Combustione
La combustione di un alcano è una reazione esotermica in cui l’alcano reagisce con l’ossigeno per dar luogo a biossido di carbonio, vapore acqueo, e calore.
Ad esempio il metano reagisce con l’ossigeno sviluppando 890 kJ/mol
Un esempio di reazione di combustione è dato dall’etano:
2 C2 H6 +7 O2 → 4 CO2 + 6 H2O
I dati sui calori di combustione degli alcani indicano che all’aumentare del numero di atomi di carbonio aumenta il calore sviluppato. Questo comportamento è dovuto al fatto che è maggiore il numero di atomi di carbonio disponibili per la combustione.
Alogenazione
In presenza di raggi U.V. avviene l’alogenazione con un meccanismo radicalico. Gli atomi di idrogeno sono sostituiti per formare una miscela di prodotti clorurati. Dalla clorurazione del metano si ottiene il clorometano secondo la reazione:
CH4 + Cl2→ CH3Cl + HCl
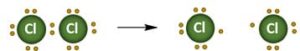
Trattandosi di una reazione che avviene per via radicalica il primo stadio, detto di iniziazione composta la scissione omolitica del legame cloro-cloro con formazione di due radicali.

Una volta che si è formato il radicale inizia la fase di propagazione in cui il radicale attacca il carbonio con formazione di un radicale sul carbonio.
Lo stadio finale della reazione, detto terminazione, può avvenire secondo diverse modalità.
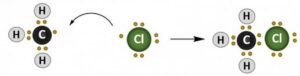
In un caso il radicale del carbonio si lega a un cloro radicale per formare l’alogenuro alchilico, come nel caso rappresentato in figura ma possono legarsi anche due radicali contenenti carbonio per dare, nella fattispecie, l’etano o possono legarsi due radicali cloro per dare Cl2.
Il clorometano è successivamente clorurato e alla fine si ottiene una miscela di clorometano, diclorometano, triclorometano e tetracloruro di carbonio.
La reazione tra alcani e fluoro è esplosiva anche al freddo e al buio, e si tende a produrre carbonio e fluoruro di idrogeno, piuttosto che la reazione di sostituzione desiderata. Non riveste particolare interesse per i chimici organici, poiché la reazione può essere molto pericolosa e non produce il prodotto desiderato.
Ad esempio, il prodotto desiderato sarebbe il fluoruro alchilico secondo la reazione:
CH4 + F2 → CH3F + HF
Tuttavia la reazione avviene così velocemente che si ottiene carbonio e HF:
CH4 + 2 F2 → C + 4 HF
Lo iodio non reagisce in alcun modo con gli alcani, almeno in normali condizioni di laboratorio mentre avviene con cloro e bromo in presenza di luce e calore
Cracking
Il cracking si realizza utilizzando pressioni e temperature elevate senza la presenza di catalizzatori oppure temperature e pressioni più basse in presenza di un catalizzatori. Il cracking è utilizzato per trasformare molecole con elevato numero di atomi di carbonio di scarso interesse commerciale in molecole con numero di atomi più piccolo
La fonte degli idrocarburi è spesso la nafta o il gasolio proveniente dalla distillazione frazionata del petrolio greggio. Queste frazioni sono ottenute dal processo di distillazione come liquide, ma vengono vaporizzate nella fase gassosa prima del cracking.
Un esempio di reazione di cracking è il seguente:
C22H46 → C10H22 + C12H26
tuttavia il frazionamento della molecola avviene in modo casuale quindi si ottengono molti prodotti



