Forze di van der Waals
Le forze di van der Waals sono forze a corto raggio presenti sia in fase gassosa che in fase liquida dovute alla fluttuazione nelle nuvole di elettroni che circondano il nucleo. Esse infatti diminuiscono, fino a scomparire all’aumentare delle distanze tra gli atomi o le molecole infatti sono significative quando le molecole sono posizionate più vicine.
Sono forze intermolecolari che possono essere dovute all’interazione dipolo-dipolo, dipolo-dipolo indotto, dipolo istantaneo-dipolo indotto dette anche forze di dispersione. A causa delle fluttuazioni nella densità di carica delle particelle un atomo o una molecola si presenta polarizzato con cariche positive a un’estremità e cariche negative all’altra e tale polarizzazione dà origine a forze elettrostatiche tra i due atomi o molecole.

Trattandosi di legami chimici secondari sono più deboli rispetto a quelli presenti in molecole in cui vi è un legame ionico o un legame covalente. Le forze di van der Waals, dovute al fisico olandese Johannes Diderik van der Waals e risalenti al 1873 possono essere di tipo attrattivo o di tipo repulsivo.
Le forze di Van der Waals sono interazioni non specifiche che possono formarsi tra qualsiasi tipo di molecola, indipendentemente dalla struttura chimica e indipendente dalla temperatura, ad eccezione delle interazioni dipolo-dipolo
Forze di van der Waals e temperature di ebollizione
Pur trattandosi di forze deboli rivestono un ruolo particolarmente importante nell’ambito della chimica organica e responsabili delle proprietà fisiche delle sostanze, come le temperature di ebollizione e di fusione.
Ad esempio, i punti di ebollizione del pentano e dell’esano sono rispettivamente di 36 e 69 °C. Ciò è dovuto al fatto che nelle molecole, entrambe molecole apolari, le forze di van der Waals sono più forti nell’esano che nel pentano perché l’esano ha una superficie maggiore per interagire con le molecole vicine.
La maggiore attrazione intermolecolare tiene insieme le molecole più strettamente, diminuendo la tensione di vapore dell’esano e conferendogli un punto di ebollizione più alto rispetto al pentano. Oltre che dalla superficie molecolare le forze di van der Waals dipendono anche dalla forma della molecola.
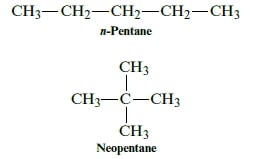
Ad esempio, il 2,2-dimetilpropano detto neopentano ha un punto di ebollizione inferiore rispetto al pentano. Il neopentano a causa della sua struttura ha una superficie inferiore rispetto a quella molecola di pentano e, di conseguenza, le forze di van der Waals sono minori nel neopentano e il suo punto di ebollizione è inferiore.
In generale, i punti di ebollizione degli alcani isomeri tra loro dipendono dalle loro forme. Un numero maggiore di ramificazioni si traduce in molecole più compatte con aree superficiali più piccole che comporta un minor contatto tra molecole adiacenti e forze di van der Waals minori. Pertanto per gli alcani isomeri tra loro quello più ramificato ha il punto di ebollizione più basso mentre quello lineare ha il punto di ebollizione più alto.
Forze di van der Waals nella vita reale
Sebbene sembrino confinate a un ambito puramente accademico e di scarsa rilevanza esse hanno una notevole importanza nella vita quotidiana soprattutto tenendo conto del fatto che la forza di attrazione, che è tipicamente compresa tra 0.4 kJ/mole e 4 kJ/mole e tende ad agire su una distanza inferiore o uguale a 0.4 nm, esiste tra atomi o molecole di una sostanza ma anche di sostanze diverse favorendone l’adesione.

Il tipico esempio è quello dei gechi, piccoli rettili che si arrampicano su superfici piane come muri e tetti dimostrando una elevata adesione superficiale delle zampe. L’area di appoggio di due zampe è di circa 22 mm², ed esse sono ricoperte da circa 3 milioni peli curvi detti setae costituiti da beta-cheratina e alfa -cheratina che producono una forza di adesione dovute a forze di interazione deboli superficiali.
Le forze di van der Waals giocano inoltre un ruolo importante nella struttura e proprietà della grafite, agiscono tra le catene idrofobiche delle proteine stabilizzandone la struttura quaternaria e tra le basi azotate del DNA.