Energia di ionizzazione: proprietà periodiche
L’energia di ionizzazione è l’energia necessaria per allontanare un elettrone da un atomo neutro allo stato gassoso:
X(g) → X+(g) + e–
Viene espressa in elettronvolt (eV) o in joule, tuttavia i valori riportati sono quelli che si riferiscono all’energia necessaria per allontanare gli elettroni da una mole di atomi e viene quindi espressa in kJ/mol.
Ad esempio l’energia richiesta per strappare un elettrone a una mole di atomi di magnesio allo stato gassoso è pari a 738 kJ:
Mg(g)→ Mg+(g) + e–
Tale valore è detto anche energia di prima ionizzazione.
Energia di seconda ionizzazione
L’energia di seconda ionizzazione è quella necessaria per allontanare un elettrone da uno ione allo stato gassoso avente una carica positiva.
I valori di energia di seconda ionizzazione sono maggiori rispetto a quelli relativi alla prima ionizzazione in quanto occorre maggior energia per allontanare un elettrone da uno ione positivo.
Ad esempio l’energia richiesta per strappare un elettrone a una mole di Mg+ allo stato gassoso è pari a 1451 kJ:
Mg+(g) → Mg2+(g) + e–
Un elemento che ha una bassa energia di ionizzazione mostra tendenza a formare cationi e sono specie riducenti.
Proprietà periodica
Essa, insieme al raggio atomico, affinità elettronica, elettronegatività e carattere metallico è una proprietà periodica.
In genere diminuisce scendendo lungo un gruppo a aumenta da sinistra a destra lungo un periodo. Questo comportamento è imputabile al fatto che scendendo lungo un gruppo l’elettrone più esterno si trova più lontano dal nucleo e quindi è più facile rimuoverlo e quindi occorre meno energia a rimuovere un elettrone dal cesio che dal litio.
Le rispettive energie di ionizzazione sono infatti rispettivamente 357.7 kJ/mol per il cesio e 520.2 kJ/mol per il litio.
L’aumento procedendo da sinistra a destra lungo un gruppo è dovuta all’aumento della carica nucleare efficace.
Piccoli discostamenti da questo trend dipendono dalle repulsioni tra gli elettroni e in particolare da quelle che interessano elettroni appartenenti allo stesso orbitale. Ad esempio l’energia di ionizzazione dell’ossigeno è minore rispetto a quella dell’azoto che lo precede nel gruppo.
Questo fenomeno è giustificato dal fatto che, mentre nell’azoto in ogni orbitale 2p è presente un elettrone, nell’ossigeno un orbitale 2p è occupato da 2 elettroni. La repulsione tra questi due elettroni rende più facile la sua rimozione.
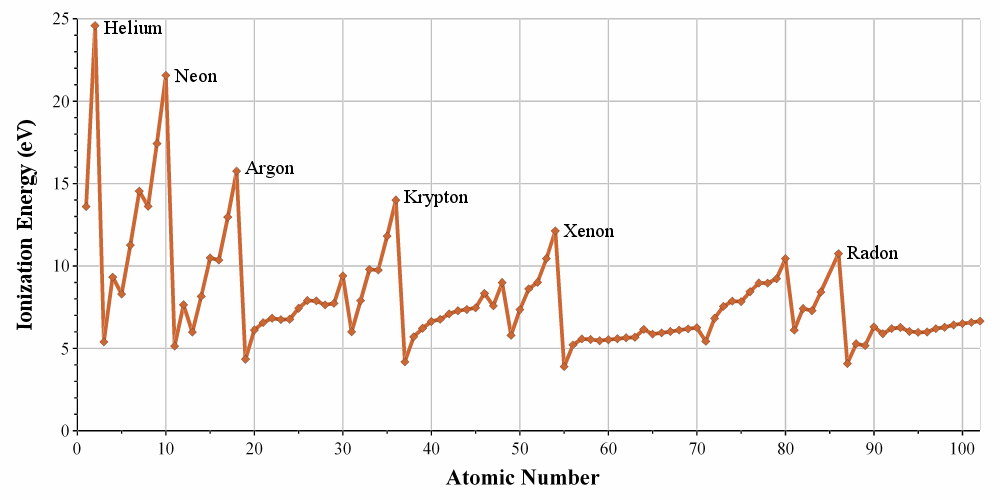
Nel grafico vengono riportate le energie di prima ionizzazione in funzione del numero atomico
Si può notare che gli elementi che hanno un maggior valore sono i gas nobili che presentano l’ottetto completo a causa della loro stabilità mentre i metalli alcalini che, perdendo un elettrone assumono la configurazione elettronica stabile del gas nobile che li precede hanno energia di ionizzazione più bassa.