Principio di Franck-Condon: transizioni elettroniche
L’interpretazione degli spettri di assorbimento elettronico si basano, tra l’altro sul principio di Franck-Condon che considera i nuclei fissi durante la transizione elettronica.
Durante la transizione elettronica quindi la geometria molecolare resta praticamente invariata. Intuitivamente, il principio risulta assai chiaro se si pensa che le masse pesanti dei nuclei non riescono a seguire subito il repentino cambiamento elettronico. Le transizioni elettroniche possono aver luogo con eccitazione simultanea di uno o più moti vibrazionali.
A temperatura ambiente è occupato il livello vibrazionale più basso (ν = 0) dello stato elettronico.
Nello stato elettronico eccitato si possono avere transizioni anche a livelli vibrazionali più alti. La presenza di parecchie transizioni vibrazionali a energie diverse ha come conseguenza un allargamento della banda di assorbimento. Nel considerare questo effetto si deve tener conto che la transizione può aver luogo tra stati elettronici che hanno la stessa distanza internucleare di equilibrio o tra stati con distanze di equilibrio diverse.
Il principio di Franck-Condon è dovuto al fisico tedesco James Franck vincitore del Premio Nobel per la Fisica nel 1925 e al fisico nucleare statunitense Edward Uhler Condon pioniere della meccanica quantistica che contribuì, nel corso della Seconda Guerra Mondiale, allo sviluppo dei radar e partecipò al progetto Manhattan
Curva di energia potenziale
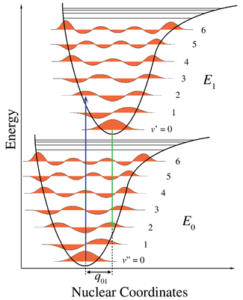
La curva di energia potenziale che mostra la variazione di energia elettronica con la distanza internucleare è rappresentata in figura.
 Principio di Franck-Condon
Principio di Franck-Condon
La discussione sulla struttura vibrazionale di una transizione elettronica si basa sul principio di Franck-Condon il quale si articola in due punti:
1) le transizioni elettroniche sono rapide ( circa 10-18 s) rispetto ai moti vibrazionali ( circa 10-12– 10-10s) in modo che la distanza internucleare rimanga invariata
2) le transizioni vibrazionali più intense si hanno nel caso in cui le regioni di alta probabilità vibrazionale si presentano, per lo stato elettronico fondamentale ed eccitato, alla stessa distanza internucleare.
Per gli stati vibrazionali la distanza internucleare più probabile è la distanza di equilibrio, mentre per quelli eccitati le distanze internucleari più probabili giacciono più vicine alla curva di energia potenziale. Quando le distanze internucleari degli stati elettronici fondamentali ed eccitati sono molto simili la transizione più intensa è la:
ν = 0 → ν’ = 0
e le transizioni a livelli vibrazionali più elevati sono meno probabili pertanto la banda vibronica, correlata ai cambiamenti dei livelli energetici vibrazionali ed elettronici che avvengono in modo simultaneo, è abbastanza stretta.
Le transizioni 1→ 1’ , 2 → 2’ ecc. possono anche risultare intense se sono occupati nello stato elettronico fondamentale livelli vibrazionali eccitati.
La distanza internucleare più elevata sia per lo stato elettronico fondamentale che per lo stato eccitato si presenta quindi quando si ha eccitazione di un elettrone da un orbitale molecolare di legame a uno di antilegame con conseguente aumento di carattere antilegante del legame stesso.
In questo caso la transizione 0 → 0’ è meno probabile e la transizione a uno degli stati vibrazionali più elevati è più intensa.
Classificazione
La classificazione più significativa che può essere fatta per le transizioni elettroniche si basa sulla natura degli orbitali molecolari coinvolti. E’ possibile così dividere le transizioni elettroniche:
1) transizioni N → V
Sono transizioni con eccitazione di un elettrone da un orbitale molecolare legante a uno antilegante e possono essere distinte in: a) σ → σ* ; b) π → π*
2) transizioni N → Q
Sono transizioni caratterizzate dal passaggio di un elettrone da un orbitale non legante localizzato su un atomo, a un orbitale molecolare antilegante. Riguardano in genere elettroni di doppietti elettronici solitari dell’azoto, ossigeno, zolfo ecc. E’ possibile distinguere queste transizioni in due tipi principali a seconda della natura dell’orbitale di arrivo, a seconda cioè che questo sia di tipo σ o π.