Orbitali di legame e di antilegame
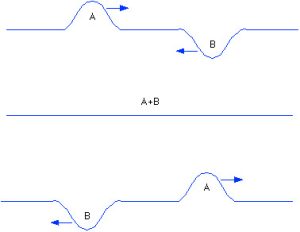
Gli orbitali di legame si formano quando gli orbitali atomici si combinano in modo che si abbiano interferenze prevalentemente di tipo costruttivo. La teoria degli orbitali molecolari tratta gli orbitali come onde e quindi quando si parla di interferenza costruttiva ci si riferisce da due onde se ne forma formazione una che è più alta delle altre due.

Orbitali di legame
Le caratteristiche principali degli orbitali di legame è che essi hanno una energia minore rispetto a quella degli orbitali atomici e la densità elettronica si addensa tra gli atomi ovvero gli elettroni hanno la massima probabilità di trovarsi tra i nuclei che costituiscono la molecola.
Il legame più forte che si può formare è il legame σ in cui la densità elettronica è centrata direttamente tra i due nuclei. Il legame σ può verificarsi per sovrapposizione di:
- due orbitali atomici s
- due orbitali p
- un orbitale s e di un orbitale p
Orbitali di antilegame
Gli orbitali di antilegame si formano quando gli orbitali atomici si combinano in modo che si abbiano interferenze prevalentemente di tipo distruttivo ovvero quando le due onde si annullano a vicenda
Le caratteristiche principali degli orbitali di antilegame è che essi hanno una energia maggiore rispetto a quella degli orbitali atomici.
Gli orbitali di antilegame inoltre presentano almeno un piano nodale ovvero una regione di spazio intorno al nucleo dell’atomo in cui è nulla la funzione d’onda e vi è la minima probabilità di trovare un elettrone. Gli orbitali di antilegame sono in genere denotati con il simbolo *
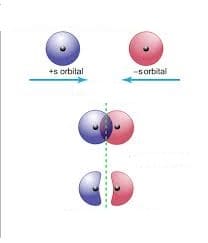
In figura è riportato un orbitale di tipo σ*
Si consideri ad esempio la molecola H2 in cui vi è un orbitale molecolare σ1s dato dalla somma delle funzioni d’onda dei due orbitali atomici 1s dell’idrogeno detti A e B:
σ1s = 1s(A) + 1s(B)
Sottraendo un orbitale atomico dall’altro si forma un piano nodale perpendicolare all’asse internucleare dove è nulla la probabilità di trovare un elettrone:
σ1s* = 1s(A) – 1s(B)
In figura vengono riportati gli orbitali molecolari relativi alla molecola di idrogeno