Tensione interfacciale e applicazioni
Si definisce tensione interfacciale la forza per unità di lunghezza presente all’interfaccia tra due fasi immiscibili. In senso più ampio, la tensione interfacciale è definita come il lavoro necessario per aumentare la dimensione dell’interfaccia tra due fasi adiacenti che non si mescolano completamente tra loro.
Il termine tensione interfacciale che si misura in dine/cm o mN/m si riferisce all’interfaccia liquido-liquido e liquido-solido, mentre per l’interfaccia liquido-gas si fa riferimento alla tensione superficiale e per l’interfaccia solido-gas si fa riferimento all’energia libera superficiale.
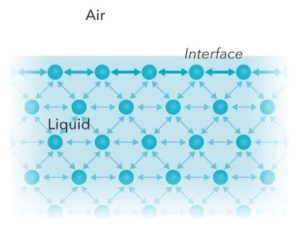
La tensione interfacciale si verifica perché una molecola vicino a un’interfaccia ha interazioni molecolari diverse rispetto a una molecola equivalente all’interno di un fluido. Pertanto le tensioni interfacciali hanno valori minori rispetto a quelli delle tensioni superficiali a causa della presenza di forze di adesione maggiori tra quelle tra le due fasi che formano all’interfaccia.
Indipendentemente dalla coppia di fasi in questione il meccanismo che provoca la forza è lo stesso. In un materiale liquido o solido, sono presenti lo stesso tipo di molecole che interagiscono tra loro nella stessa maniera. All’interfaccia le molecole interagiscono con quelle della stessa specie tramite forze di coesione.
Nei sistemi aria-liquido e specialmente nei sistemi aria-solido queste forze coesive possono essere molto forti, con conseguenti valori elevati di tensione superficiale ed energia libera superficiale. Tuttavia, quando sono in contatto due liquidi immiscibili o liquido e solido, anche le forze di adesione tra le molecole diverse svolgono un ruolo significativo e bilanciano le forze all’interfaccia.
Tensione interfacciale e equazione di Young
L’equazione di Young proposta nel 1805 dovuta allo scienziato britannico Thomas Young fu stabilita assumendo che esista una superficie solida ideale con proprietà lisce, inerti, indeformabili e omogenee, e la gocciolina liquida è identificata come un’entità coerente. Quando la goccia di un liquido è posta su una superficie, il sistema tende a raggiungere uno stato di equilibrio con energia minima.

Detta γ la tensione superficiale riferita all’energia specifica alle interfacce che riflette la forza coesiva della fase condensata sottostante secondo l’equazione di Young:
cos θγ = γsv – γsl/ γlv
dove θγ rappresenta l’angolo di contatto all’equilibrio, γsv la tensione di interfaccia tra solido e vapore, γs la tensione di interfaccia solido liquido e γlv la tensione interfacciale liquido vapore. Nell’equazione gioca quindi il ruolo fondamentale della tensione di interfaccia ma la bagnabilità delle superfici solide è influenzata anche da altri parametri quali rugosità e eterogeneità.
Dall’equazione di Young si comprende che questo quando una goccia di liquido è posta su una superficie solida, il suo perimetro si sposta, allargandosi o contraendosi, fino a quando l’angolo θ assume il valore dato dall’equazione.
Applicazioni industriali
Le misurazioni della tensione interfacciale tra due liquidi immiscibili sono utilizzate in diverse aree industriali come, ad esempio, la lavorazione del petrolio greggio nell’industria petrolifera. Il petrolio greggio è per lo più presente come un’emulsione di acqua, in cui vi sono sostanze organiche e inorganiche disciolte, e di fase non acquosa.

Si rende quindi necessario allontanare l’acqua prima del processo di raffinazione. Se due liquidi immiscibili sono in contatto tra loro, tenderanno a mantenere un’interfaccia il più piccola possibile poiché l’energia interfacciale è associata alla formazione di qualsiasi area interfacciale. Di conseguenza, è molto difficile mescolare i due liquidi. Quando vengono agitati insieme, si formeranno goccioline sferiche, poiché i liquidi tendono a mantenere un’area superficiale il più piccola possibile e verrà mantenuta una tensione interfacciale tra i due liquidi.
Tuttavia quando le emulsioni sono stabili risulta particolarmente complesso separare le due fasi. Tuttavia se la tensione interfacciale viene ridotta l’emulsione perde stabilità ed è quindi possibile separare la fase acquosa. Questa operazione può essere fatta utilizzando opportuni tensioattivi, che consentono alla fase organica di essere mobilizzata dopo l’allagamento con acqua.



