Tautomeria: protonica, cheto-enolica
La tautomeria, scoperta dal fisico tedesco Johannes van Laar è quel fenomeno che permette l’esistenza di strutture isomere, in equilibrio tra loro che differiscono per la posizione relativa dei loro atomi e derivano dalla rottura di legami e dalla formazione di legami σ.
A differenza della risonanza, quindi, si tratta di una vera e propria reazione chimica in cui un frammento si stacca dal resto della molecola per riagganciarsi ad essa in una posizione diversa. Le forme tautomeriche non vanno confuse con le forme di risonanza che, al contrario, non hanno una reale esistenza fisica.
Tautomeria protonica
Il tipo più comune di tautomeria è la cosiddetta tautomeria protonica, in cui si stabilisce un equilibrio tra due o più forme che differiscono tra loro per la posizione a cui è legato il protone come si può osservare in figura:
Tautomeria cheto-enolica
Lo stesso tipo di equilibrio, riferito, però a un chetone con idrogeni in α al carbonile, porta alla cosiddetta tautomeria cheto-enolica:

La composizione della miscela di equilibrio è controllata da vari fattori tra cui pH, temperatura e tipo di solvente. L’interconversione cheto-enolica è soggetta sia a catalisi acida ed avviene in due stadi:
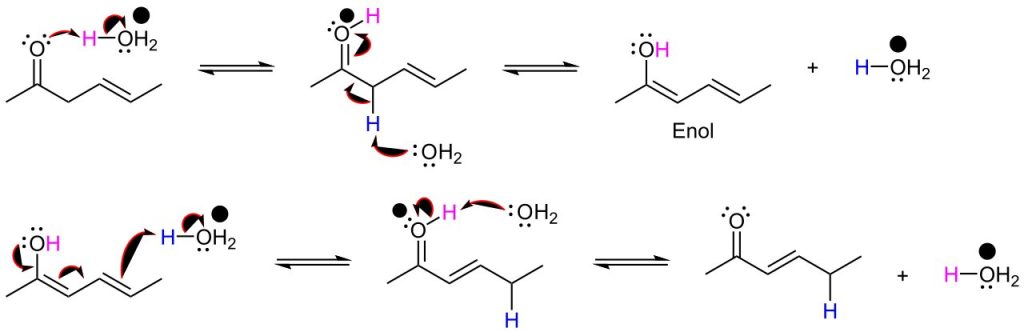 1° stadio: nel primo stadio un protone si lega all’ossigeno carbonilico con formazione dell’acido coniugato del composto carbonilico
1° stadio: nel primo stadio un protone si lega all’ossigeno carbonilico con formazione dell’acido coniugato del composto carbonilico
2° stadio: nel secondo stadio una molecola di acqua agisce da base secondo Bronsted-Lowry e rimuove un protone dal carbonio in α all’aldeide o al chetone protonato con formazione dell’enolo
In alternativa l’interconversione cheto-enolica può essere soggetta a catalisi basica. La base estrae il protone dal carbonio in α al carbonile generando l’anione enolato che può protonarsi all’ossigeno per dare l’enolo.
Eccetto che in completa assenza di acido o di base le forme cheto-enoliche sono in rapida interconversione tra loro.
Quindi esistono in un equilibrio mobile, la cui posizione dipende:
- dai dettagli strutturali del composto
- dalle condizioni sperimentali in cui si trova (solvente, temperatura, concentrazione, pH ecc.).
Equilibrio
Per quanto riguarda l’equilibrio cheto-enolico si può dire che, in genere, la forma carbonilica è più stabile. Per le aldeidi e i chetoni più semplici l’equilibrio è fortemente spostato dalla parte della forma chetonica come nel caso dell’acetone la forma enolica è presente allo 0.00025%.
Tuttavia, se per esempio, il doppio legame dell’enolo si coniuga con un gruppo in grado di delocalizzare elettroni per risonanza o se una certa stabilizzazione può essere derivata dalla formazione di legami a idrogeno la forma enolica può essere presente in quantità più rilevante.

La risonanza può avere una certa influenza nella determinazione della posizione all’equilibrio. Oltre alla delocalizzazione e alla possibilità di formare legami a idrogeno altri fattori possono essere importanti per definire la percentuale di forma chetonica e forma enolica. Per esempio, la scarsa tendenza a enolizzare del diacetile è attribuita alla necessità della molecola di assumere una disposizione trans a causa della forte repulsione esistente tra i dipoli.
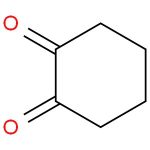
Al contrario il cicloesan 1,2 dione che non può eliminare questo elemento di instabilità per rotazione intorno al legame che unisce i due carbonili, lo elimina convertendosi completamente, allo stato puro, nella forma enolica
Anche il solvente ha un ruolo importante nel controllare la posizione dell’equilibrio cheto-enolico.
In un solvente che può formare legami a idrogeno come l’acqua, la percentuale di forma enolica si riduce in maniera piuttosto drastica. L’acetilacetone, ad esempio si trova per il 95% in forma enolica se il solvente è l’esano. Si trova, in forma enolica per il 5% se il solvente è l’acqua.
Le forme enoliche di molti composti dicarbonilici esistono in strutture cicliche intramolecolari a legami idrogeno denominate anelli chelati. Sali chelati di particolare stabilità possono essere formati fra enoli di composti dicarbonilici e vari ioni metallici. Per la coordinazione è necessario che lo ione metallico abbia orbitali vuoti a basso livello come nel caso del rame.




