Risonanza magnetica nucleare del 13 C: chemical shift
La spettroscopia di risonanza magnetica nucleare si basa sulle perturbazioni dei livelli energetici dei nuclei sotto l’effetto di un forte campo magnetico. Le due caratteristiche macroscopiche dei nuclei sono la massa M e la carica Z; i nuclei, tuttavia, hanno altre proprietà quali la distribuzione della carica che è in diretta relazione con le loro proprietà magnetiche in quanto alcuni nuclei sono dotati di spin che possono essere rappresentati come una rotazione del nucleo intorno ad un asse.
Un nucleo dotato di spin è quindi paragonabile a un ago magnetico il sui asse coincide con l’asse di spin del nucleo. Ad ogni nucleo può quindi essere associato un caratteristico momento magnetico nucleare il cui verso è parallelo a quello del momento della quantità di moto (momento angolare).
Ogni nucleo è caratterizzato da un numero quantico di spin I
Tabella
Numero di protoni | Numero di neutroni | Spin (I) | Esempio | |
| Pari | Pari | Pari | 0 | 16O |
| Dispari | Dispari | Numero intero (1,2,..) | 2H | |
| Dispari | Pari | Dispari | Numero frazionario (1/2 , 3/2…) | 13C |
| Dispari | Pari | Numero frazionario (1/2 , 3/2…) | 15N |
Quando I = 0 il nucleo non ha momento magnetico, quando I = 1/2 il nucleo ha un momento angolare non nullo, mentre quando I > 1/2 il nucleo non solo è dotato di momento magnetico, ma anche di momento elettrico. Si può concludere che tutti i nuclei che hanno lo stesso valore del momento magnetico di spin hanno lo stesso valore del momento angolare di spin malgrado le diverse masse.
Quando un nucleo è immerso in un campo magnetico omogeneo esterno Ho si genera un’interazione magnetica tra il suo momento angolare di spin e il campo magnetico e tale interazione è sfruttata dalla spettroscopia di risonanza magnetica nucleare.
La spettroscopia NMR del protone rappresenta per il chimico organico il mezzo più importante per l’interpretazione e la determinazione di una struttura. Tuttavia, possono essere presenti in una molecola parti in cui mancano legami C-H e pertanto lo spettro risulta poco utile.
Tenendo conto del fatto che tutti i composti organici contengono carbonio e che l’isotopo 13C che ha uno spin nucleare uguale a 1/2 costituisce circa l’1.1% del carbonio presente in natura è stata realizzata la spettroscopia di risonanza magnetica nucleare del carbonio 13 che dà indicazioni relative sia alla struttura di molecole organiche che allo studio delle reazioni organiche.
Interpretazione della risonanza magnetica 13C
I fattori che determinano i Chemical Shifts sono complessi. Tuttavia lo spostamento chimico di un atomo di carbonio è influenzato dall’elettronegatività degli atomi vicini. Gli atomi di carbonio legati all’ossigeno, all’azoto o all’alogeno assorbono verso il basso (a sinistra) i tipici carboni degli alcani.
Poiché gli atomi elettronegativi attraggono gli elettroni, li allontanano dagli atomi di carbonio vicini, provocando la deschermatura di tali atomi di carbonio e l’entrata in risonanza in un campo inferiore.
Un’altra tendenza è che gli atomi di carbonio ibridati sp3 assorbono generalmente da 0 a 90 δ , mentre gli di carbonio sp2 assorbono da 110 a 220 δ . Gli atomi di carbonio del gruppo carbonilico (C=O) sono particolarmente distinti nella risonanza magnetica 13C e si trovano sempre all’estremità del campo basso dello spettro, da 160 a 220 δ .
Spettro 13C
In particolare lo spettro 13C di un composto organico dà informazioni relative a:
– diversi tipi di carbonio presenti in una molecola
– l’intorno dei diversi atomi di carbonio
– il numero di atomi di carbonio che si trovano legati a un determinato atomo di carbonio
Vengono riportati i chemical shifts del carbonio 13 in tetrametilsilano:
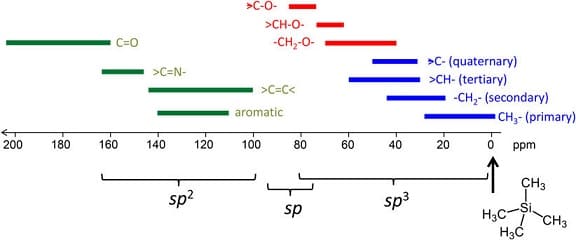
Tale tipo di spettroscopia, tuttavia, ha maggiori complicazioni rispetto alla spettroscopia protonica ed è meno sensibile la minore percentuale di 13C presente nel carbonio (1.1%) rispetto a quella dell’1H che costituisce il 99.985% della quantità di idrogeno totale



