Butano: isomeria, reazioni, usi
Il butano è un alcano con quattro atomi di carbonio e quindi ha formula C4H10.
Come in tutti gli alcani che sono composti saturi ovvero non contengono doppi legami carbonio -carbonio gli atomi di carbonio sono ibridati sp3
È il primo degli alcani a mostrare isomeria di catena. Esso infatti può avere:
- struttura lineare CH3CH2CH2CH3 detto n-butano
- struttura ramificata CH3CH(CH3)2 detto isobutano o metilpropano
Entrambi gli isomeri del butano si trovano nel gas naturale e nel petrolio greggio e si ottengono dalla raffinazione del petrolio.
È un gas incolore facile da liquefare avendo una temperatura di liquefazione prossima a 0 °C ed è scarsamente solubile in acqua.
Isomeria conformazionale del butano
Come per i composti aciclici anche il butano mostra isomeria conformazionale.
Essa è dovuta al fatto che esiste una barriera energetica sia pure dell’ordine di poche kcal/mol per la rotazione intorno al legame semplice.
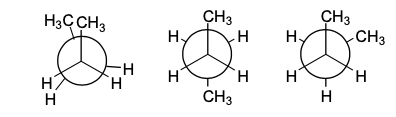
Se l’angolo è 60° la forma è sfalsata e si ha un minimo di energia. Un’altra conformazione eclissata si ha a 120° e un arrangiamento sfalsato a 180°. La conformazione a 60° è detta gauche mentre quella a 180° è detta anti.
Poiché nella conformazione gauche i gruppi metilici sono abbastanza tra loro in modo da esercitare delle repulsioni di tipo van der Waals, l’energia della forma gauche è circa 0.8 kcal/mol maggiore di quella della forma anti.
Sintesi
Il butano può essere ottenuto mediante la reazione di Wurtz, dovuta il chimico francese Charles-Adolphe Wurtz che in cui viene fatto reagire un alogenuro alchilico come il bromoetano con sodio metallico in presenza di etere anidro:
2 C2H5Br + 2 Na → CH3CH2CH2CH3
Può essere ottenuto dalla distillazione frazionata del petrolio greggio. In lavoratorio può essere ottenuto
Reazioni
Esso dà le reazioni tipiche degli alcani ovvero combustione e alogenazione.
La reazione di combustione:
2 CH3CH2CH2CH3 + 13 O2→ 8 CO2 + 10 H2O
Ha un’entalpia di – 2877.5 kJ/mole e pertanto la reazione è esotermica.
L’alogenazione avviene secondo un meccanismo radicalico che può portare alla sostituzione di tutti gli atomi di idrogeno e dà generalmente, come prodotto di reazione una miscela di alogenuri alchilici.
Usi
Il butano, che è uno dei componenti del GPL è utilizzato come combustibile. Per questa sua prerogativa è usato nei fornelli da campeggio
Costituisce una delle materie prime per la produzione della gomma sintetica.
Inoltre è usato in deodoranti e nelle bombolette spray come propellente e negli impianti di condizionamento.
Viene utilizzato come detergente in settori come l’elettronica e l’ottica per rimuovere sporco, grasso e olio. Il butano può essere utilizzato come additivo per la benzina per aumentarne la volatilità.


