Esaboruro di lantanio
L’esaboruro di lantanio è un eccellente materiale ceramico che presenta un elevato punto di fusione, elevata durezza, eccellente stabilità termica, bassa pressione di vapore, elevata conduttività elettrica, conduttività termica e basso coefficiente di dilatazione termica.
L’esaboruro di lantanio è un boruro inorganico con formula LaB6 costituito dal boro, non metallo del blocco p appartenente al Gruppo 13 e al 2° Periodo avente configurazione elettronica 1s2,2s2,2p1 e da lantanio, metallo capostipite della serie dei lantanidi o delle terre rare che ha configurazione elettronica [Xe] 5d1 6s2 scoperto dal chimico svedese Carl Gustaf Mosander nel 1839.
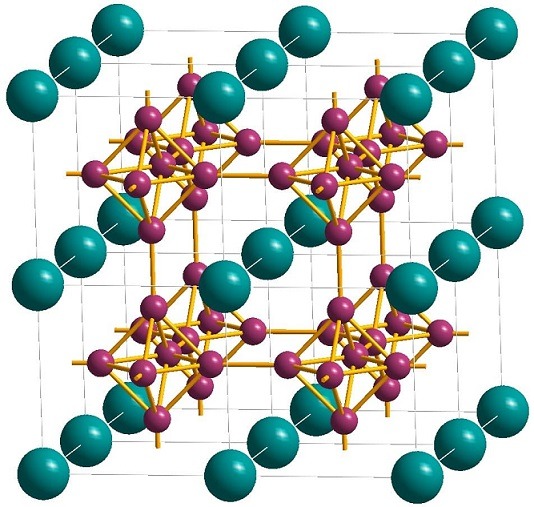
Tra gli esaboruri delle terre rare, l’esaboruro di lantanio possiede la pressione di vapore più bassa e presenta una struttura reticolare cubica di tipo CsCl in cui l’atomo di lantanio si trova al centro e otto atomi di boro si trovano simmetricamente nell’angolo del cubo
Sintesi dell’esaboruro di lantanio
L’esaboruro di lantanio viene solitamente prodotto mescolando La e B con alluminio in un forno a 1500 K da cui si ottengono cristalli di grandi dimensioni. Boro e lantanio ad elevata purezza vengono miscelati insieme e riscaldati in un crogiolo in atmosfera inerte per diverse ore, per garantire una miscelazione omogenea. Questo metodo, tuttavia, non è adatto alla produzione di nanocristalli.
Metodi sintetici alternativi prevedono la reazione dell’idruro di lantanio (II) LaH2 con il boro o tramite reazione del cloruro di lantanio (III) LaCl3 in presenza di sodio alluminio idruro e magnesio. Un altro metodo prevede l’elettrolisi di un sale fuso utilizzando un sale contenente ossido di lantanio (III) La2O3, anidride borica B2O3, fluoruro di litio LiF e ossido di litio Li2O.
L’esaboruro di lantanio può essere ottenuto anche facendo reagire cloruro di lantanio (III), LaCl3 con cloruro di boro BCl3 e idrogeno gassoso. Altri metodi prevedono la riduzione borotermica dell’ossido di lantanio in presenza di boro, la riduzione carbotermica dell’ossido di lantanio con boro e carbonio.
Tali tecniche, che richiedono temperature tra 1400 e 1800 °C, sono comunemente utilizzate nell’industria, poiché sono semplici e danno reazioni chimiche dirette in fase solida tra i reagenti facilmente disponibili. Un altro metodo prevede la reazione tra ossido di lantanio e carburo di boro secondo la reazione:
La2O3 + 3 B4C → 2 LaB6 + 3 CO
Un metodo per ottenere esaboruro di lantanio nanostrutturato prevede la reazione in fase solida a bassa temperatura di un composto di lantanio come ossido, idrossido, ossalato o nitrato di lantanio, un agente riducente metallico come polvere di magnesio, di alluminio, di zinco o di ferro, un agente alogenante come bromuro di boro, pentacloruro di fosforo, cloruro di ammonio, cloruro di magnesio o cloruro di calcio e un composto di boro come ossido, borace, acido metaborico e sodio boroidruro.
Proprietà
L’esaboruro di lantanio si presenta sotto forma di polvere di colore viola quando si trova in quantità stechiometrica mentre se è ricco di boro, al di sopra di 6.07 appare blu. Se subisce un bombardamento ionico assume una colorazione blu.

Ha una durezza, nella scala di Mohs di 9.5. A causa della sua struttura in cui gli atomi di boro sono legati in modo covalente ha un elevato punto di fusione pari a 2210 °C per la forza di tali legami.
È stabile e dotato di una buona resistenza chimica pertanto non reagisce con l’acqua, l’ossigeno e con l’acido cloridrico ma, a temperatura ambiente, reagisce con acido nitrico e acqua regia. Ha un basso valore (circa 2.6 eV ) della funzione lavoro detta anche lavoro di estrazione che è l’energia minima che occorre fornire per estrarre un elettrone e pertanto trova utilizzo come emettitore termoionico di elettroni.
Usi
L’esaboruro di lantanio viene utilizzato catodo negli emettitori termoionici per realizzare cannoni elettronici, che sono una parte indispensabile dei microscopi usati nella microscopia elettronica a scansione, dei microscopi elettronici a trasmissione e dei sistemi di litografia elettronica.

Inoltre è un promettente superconduttore e assorbitore solare e viene utilizzato come additivo per migliorare la resistenza all’ossidazione dei materiali a temperature estreme. È stata inoltre sviluppata una tecnica di montaggio per catodi di esaboruro di lantanio policristallini e monocristallini per i gruppi di filamenti standard di varie sorgenti ioniche.
Tra i vantaggi sembrano figurare una temperatura inferiore della sorgente ionica, un aumento dell’efficienza della ionizzazione e una durata prolungata che potrebbe portare all’analisi di composti termicamente instabili.



