Ibridazione dell’azoto: esempi
L’ibridazione dell’azoto varia a seconda dei tipi di composti.
L’azoto è presente in molti composti organici come ammine, ammidi, immine, immidi, cianati, isocianati, nitrili, isonitrili e in molti eterocicli sia aromatici che non aromatici.
Esso ha numero atomico 7 e quindi ha configurazione elettronica 1s2,2s2,2p3 e presenta tre elettroni spaiati negli orbitali p e un doppietto elettronico solitario nell’orbitale s.
Come il carbonio anche l’azoto può formare orbitali ibridi sp3 , sp2 e sp. La conoscenza dell’ibridazione di un elemento in una molecola consente la previsione della geometria molecolare.
Esempi
In alcuni composti, come, ad esempio la metilammina, è facile prevedere l’ibridazione dell’azoto andando per analogia con l’ibridazione dell’azoto nell’ammoniaca.
Nell’ammoniaca infatti l’azoto forma 4 orbitali ibridi sp3 uno dei quali è occupato dal doppietto elettronico solitario.
In composti come la metilammina due orbitali si sovrappongono con i rispettivi orbitali atomici 1s dell’idrogeno e l’ultimo orbitale si sovrappone a uno degli orbitali ibridi sp3 del carbonio formando 3 legami σ

Anche nel caso dell’etanonitrile noto come acetonitrile in cui è presente un triplo legame carbonio-azoto è facile prevedere l’ibridazione dell’azoto. Quest’ultimo forma 2 legami π e un legame σ con il carbonio centrale ed è pertanto ibridato sp.

Anche nel caso della pirrolidina
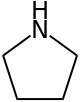
che è un eterociclo saturo evidentemente non aromatico è facile attribuire all’azoto ibridazione sp3.
Per quanto attiene il 2,3-diidropirrolo

la situazione diventa più complicata. In tali casi può giungere un suggerimento considerando se vi è un incremento di risonanza, coniugazione o aromaticità in caso di presenza di un orbitale p dell’azoto che comporta quindi una ibridazione sp2 l’azoto presenta questo tipo di ibridazione.
Nel caso della specie in esame si ha un aumento di coniugazione pertanto l’azoto è ibridato sp2 e l’orbitale p entra a far parte di un sistema coniugato.



