Equazione di Maxwell-Boltzmann: velocità molecolari
L ‘equazione di Maxwell-Boltzmann, che costituisce la base della teoria cinetica dei gas, definisce la distribuzione delle velocità per un gas a una certa temperatura. Da questa funzione di distribuzione è possibile derivare la velocità più probabile, la velocità media e la velocità quadratica media
Secondo i postulati dell’energia cinetica, le particelle gassose si muovono con velocità diverse sia per modulo sia per direzione e verso e cambiano continuamente per effetto degli urti. Pertanto se non è possibile conoscere la velocità delle singole particelle, è invece possibile calcolare statisticamente la frazione di particelle che ha una velocità compresa tra un qualunque valore v e v + dv indipendentemente dalla direzione e verso. Il risultato del calcolo è espresso dalla relazione di Maxwell-Boltzmann:
dn/N = 4 π ( m/ 2π kT)3/2 v2 dv e-mv2/ 2 kT
Figura
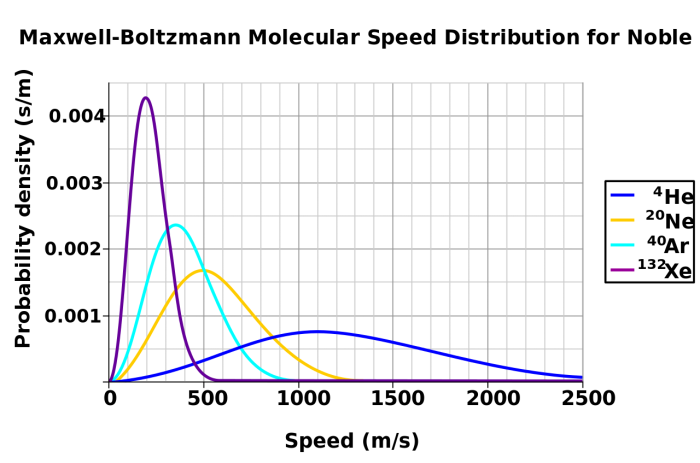
è riportato come varia la frazione di particelle rispetto a quelle totali che hanno una velocità compresa tra v e v + dv, dove dv è un incremento unitario della velocità.
Questa finzione assume valore uguale a zero quando v = 0 e tende a zero quando la velocità tende a infinito e assume valori positivi finiti per qualunque altro valore della velocità. La funzione assume il valore massimo a una velocità che rappresenta la velocità posseduta dalla frazione relativamente più grande di particelle e, quindi, rappresenta la velocità più probabile (vpp).
Poiché la curva non è simmetrica rispetto alla retta parallela all’asse delle ordinate e passante per vpp e quindi l’area della superficie definita dalla curva e dall’asse delle ascisse a destra è maggiore di quella di sinistra, la frazione di particelle che ha velocità maggiore di quella più probabile è maggiore di quella che ha una velocità minore di quella più probabile per cui la velocità media delle particelle è maggiore di quella più probabile. Il valore della velocità più probabile vpp si ricava dalla precedente equazione differenziandola e ponendo la derivata uguale a zero:
vpp = √(2 kT/m)
La velocità media si ottiene dall’espressione v dv/N con v che va da 0 a + ∞ che porta a v = √(8 kT/πm)
La maggior parte delle particelle ha una velocità vicina a quella più probabile, o poco più grande o poco più piccola, mentre è piccola la frazione di particelle che ha velocità molto differente da questa.
Grafico
La curva della figura si riferisce a un sistema gassoso a temperatura costante; a mano a mano che la temperatura aumenta si ha un appiattimento della curva e, di conseguenza, uno spostamento verso destra sia della velocità più probabile che di quella media:
un aumento di temperatura ha quindi l’effetto di aumentare la velocità delle particelle ed inoltre, a mano a mano che la curva si appiattisce, una stessa frazione di particelle è distribuita è distribuita entro un intervallo di velocità sempre più ampio. L’espressione della distribuzione di energia cinetica translazionale, la sola energia posseduta da un gas ideale, è:
dn/N = 2π ( 1/π kT)3/2 E1/2 e-E/kT dE
nella figura è riportata la rappresentazione grafica di questa funzione:
essa è analoga, ma non identica, alla curva di distribuzione delle velocità. Anche in questo caso l’energia più probabile Epp è minore di quella media ed inoltre un aumento della temperatura fa aumentare sia l’una che l’altra. Dalla legge di distribuzione dell’energia si può calcolare la frazione di particelle che ha energia maggiore di un qualsiasi valore E*: questa frazione aumenta rapidamente all’aumentare della temperatura, mentre per una stessa temperatura diminuisce a mano a mano che aumenta il valore di E*.