Carica formale: determinazione, esempi
La carica formale è la carica assegnata a un atomo presente in una molecola o in uno ione poliatomico assumendo che gli elettroni di legame siano equamente condivisi a prescindere dall’elettronegatività di ciascun atomo.
Una molecola o uno ione poliatomico rappresentati da più strutture di Lewis essa è utile per stabilire quale fra queste strutture meglio rappresenta i legami della molecola e per poter prevedere la reattività.
Determinazione della carica formale
Ci si può avvalere della seguente formula:
Carica formale = ( numero di elettroni di valenza dell’atomo neutro) – (numero degli elettroni di valenza di non legame dell’atomo nella molecola) – ½ ( numero di elettroni presenti nei legami covalenti).
In una molecola la carica formale complessiva deve essere uguale a zero mentre in uno ione poliatomico deve essere pari alla carica dello ione
Esempi
Ad esempio nel caso della molecola di anidride carbonica le possibili strutture di Lewis sono indicate in figura:
Per identificare quale delle due strutture sia più rappresentativa calcoliamo per entrambe la carica formale:
per la prima delle due formule la carica formale di entrambi gli atomi di ossigeno è data da: 6 – 4 – ½ (4) = 0
per il carbonio è data da: 4 – 0 – ½ ( 8) = 0
Per la seconda struttura quella dell’ossigeno scritto a sinistra vale 6 – 6 – ½ (2) = -1
Quella dell’ossigeno scritto a destra vale 6 – 2- ½ (6) = +1
Per il carbonio è data da: 4 – 0 – ½ ( 8) = 0
Si noti che essa in entrambe le strutture è pari a zero a conferma che CO2 è una molecola neutra, ma la struttura che presenta una struttura di Lewis simmetrica in cui entrambi gli atomi di ossigeno hanno carica formale 0 appare più stabile dell’altra in cui uno dei due atomi di ossigeno (elemento più elettronegativo del carbonio) ha carica formale +1.
Calcoliamo ora quella dell’azoto nell’ammoniaca la cui struttura di Lewis è rappresentata in figura:

azoto = 5 – 2 – ½(6)= 0
idrogeno = 1 – 0 – ½ (2) = 0
Come esempio di uno ione poliatomico consideriamo lo ione H3O+ la cui struttura di Lewis è rappresentata in figura:
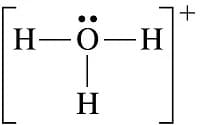
ossigeno = 6 – 2 – ½ ( 6) = +1
idrogeno = 1 – 0 – ½ (2) = 0
La carica formale dello ione poliatomico è quindi +1



