Acqua pesante: proprietà, usi
L’acqua pesante, detta anche ossido di deuterio, contiene solo deuterio ed è indicata come 2H2O o come D2O. Si trova in natura in quantità irrisorie rispetto a quella che contiene il protio e, poiché il deuterio è un isotopo stabile, lo è anche l’acqua pesante che pertanto non è radioattiva.
Il chimico statunitense Gilbert Lewis nel 1933, a due anni dalla scoperta del deuterio, isolò per la prima volta l’acqua pesante
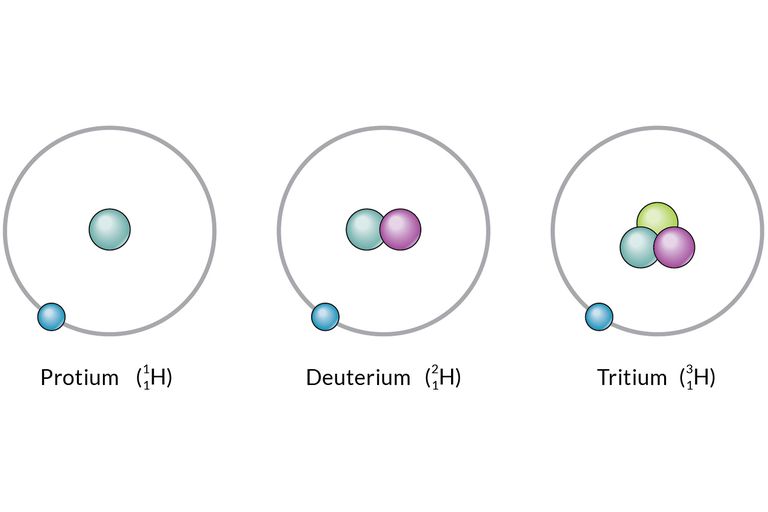
L’idrogeno si presenta sotto tre forme isotopiche che, per la loro importanza, assumono nomi diversi contrariamente agli altri atomi per i quali gli isotopi vengono solo indicati tramite numero atomico e numero di massa.
Gli isotopi dell’idrogeno sono il protio che ha un solo protone e nessun neutrone, il deuterio che ha un protone e un neutrone e il tritio che ha un protone e due neutroni.
I due isotopi stabili sono il protio che ha un’abbondanza relativa del 99.985% e il deuterio che ha un’abbondanza relativa dello 0.015%.
Proprietà dell’acqua pesante
La sostituzione dell’idrogeno con il deuterio varia le proprietà chimiche e fisiche dell’acqua pesante rispetto all’acqua come, ad esempio temperatura di congelamento, di ebollizione, densità e pH.
A pressione atmosferica, ha una temperatura di ebollizione di 101.4 °C rispetto all’acqua che ha una temperatura di ebollizione di 100°C. Grazie a questa differenza può essere prodotta per distillazione sebbene il processo sia lungo e necessiti di colonne con elevato numero di piatti.
Oltre che per via elettrolitica l’acqua pesante è prodotta tramite il processo Girdler che si basa su uno scambio isotopico tra H2S e H2O.
Usi
L’acqua pesante è utilizzata quale:
- moderatore dei neutroni nei reattori nucleari ad acqua pesante
- solvente deuterato
- fonte di deuterio per ottenere isotopi marcati selettivamente.
- E’ usata per avere indicazioni relative ai meccanismi di reazione e per la spettroscopia NMR
Da essa si possono inoltre ottenere farmaci deuterati alcuni dei quali già approvati in quanto possono essere metabolizzati in maniera diversa rispetto a farmaci già noti.