Elettrodo a calomelano: semireazioni, potenziale
L’ elettrodo a calomelano è un elettrodo di riferimento costituito da mercurio su cui viene stratificata una pasta di mercurio e del sale poco solubile cloruro di mercurio (I) Hg2Cl2. Quest’ultimo è detto calomelano ed è a contatto con una soluzione contenente ioni cloruro.
Nel 1788 il chimico Carl Wilhelm Scheele inventò il metodo per produrre il calomelano per precipitazione. La soluzione contiene l’anione presente nel sale poco come ad esempio una soluzione satura di KCl.
Abitualmente è utilizzato un filo di platino per consentire il contatto con il circuito esterno
Schema della semicella contenente l’elettrodo a calomelano
La semicella contenente l’elettrodo può essere schematizzata come:
Hg│ Hg2Cl2│Cl–
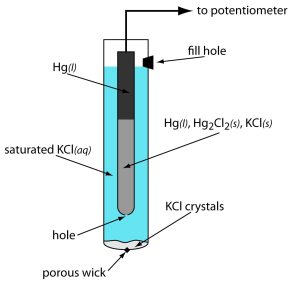
L’elettrodo può fungere da anodo o da catodo a seconda della natura dell’altro elettrodo presente nella cella.
Quando agisce da anodo la semireazione di ossidazione è:
2 Hg + 2 Cl– → Hg2Cl2 + 2 e–
Quando agisce da catodo la semireazione di riduzione è:
Hg2Cl2 + 2 e– → 2 Hg + 2 Cl–
L’equazione di Nernst relativa a quest’ultima semireazione è:
E = E° + 0.059/2 log 1/[Cl–]2
Essendo pari a due il numero di elettroni coinvolti nella semireazione e tenendo conto del fatto che sia Hg2Cl2 che Hg sono allo stato solido e pertanto non compaiono nell’equazione.
L’equazione di Nernst può essere riarrangiata come:
E = E° – 0.059/2 log [Cl]2
Ovvero
E = E° – 0.059 [Cl–]
Essendo E° = 0.27 V
Potenziale di riduzione
Il potenziale di riduzione di un elettrodo a calomelano dipende quindi dalla concentrazione dello ione cloruro.
Esistono in commercio vari tipi di elettrodo a calomelano tra cui quello a calomelano saturo ovvero a contatto con una soluzione satura di KCl. Per poter calcolare il potenziale di questo elettrodo bisogna conoscere la solubilità di KCl che è pari a 342 g/L.
Pertanto la concentrazione molare della soluzione è pari a 342 g/L/74.55 g/mol= 4.59 M
Il potenziale dell’elettrodo vale quindi E = + 0.27 – 0.059 log 4.59 = 0.23 V
L’elettrodo a calomelano non può essere utilizzato a temperature superiori a 50°C a cui avviene una reazione di disproporzione:
Hg2Cl2 → Hg + HgCl2
In cui il mercurio passa da numero di ossidazione +1 a numero di ossidazione 0 e +2
A causa della tossicità del mercurio viene attualmente preferito l’elettrodo ad Argento/Cloruro di argento



