Cicloossigenasi
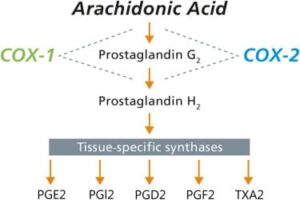
La cicloossigenasi (COX) o prostaglandina endoperossido sintasi (PGHS) è l’enzima chiave nella sintesi delle prostaglandine, a partire dal loro precursore, l’acido arachidonico. Le due isoforme della cicloossigenasi, dette COX-1 e COX-2, sono i bersagli dei farmaci antinfiammatori non steroidei (FANS) ampiamente utilizzati, pertanto questi enzimi hanno un ruolo nel dolore, nella febbre e nell’infiammazione.
Lo studio delle prostaglandine ha portato a chiarire il meccanismo d’azione dell’aspirina che ne inibisce la sintesi. Il biochimico e farmacologo britannico, premio Nobel per la medicina nel 1982 John Vane dimostrò nel 1971 che i farmaci antinfiammatori non steroidei bloccavano la cicloossigenasi.
Nel 1991, Daniel Simmons, direttore del Centro di ricerca sul cancro della Brigham Young University, descrisse il gene che esprime una seconda cicloossigenasi, la COX-2. Questa scoperta spiega le azioni antinfiammatorie dei FANS, l’inibizione della cicloossigenasi 2 e della cicloossigenasi 1
Struttura delle cicloossigenasi
La COX-1 e la COX-2 umane sono omodimeri costituite da 576 e 581 amminoacidi, rispettivamente. Entrambi gli enzimi contengono tre oligosaccaridi ad alto contenuto di mannosio, uno dei quali facilita il folding delle proteine e un quarto oligosaccaride, presente solo nella COX-2, ne regola la degradazione.
Le strutture tridimensionali della COX-1 e della COX-2 sono quasi sovrapponibili. Ciascuna subunità del dimero è costituita da tre domini, il dominio del fattore di crescita epidermico (residui 34–72), il dominio di legame alla membrana (residui 73–116) e il dominio catalitico che comprende la maggior parte della proteina, che contiene la cicloossigenasi e la perossidasi siti attivi su entrambi i lati del gruppo protesico dell’eme.
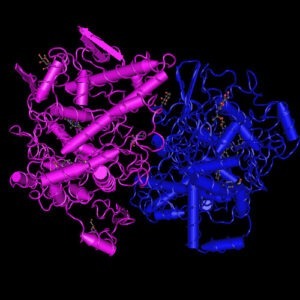
Il monomero della cicloossigenasi è costituito da tre domini strutturali distinti ma funzionalmente e strutturalmente interconnessi: un dominio simile al fattore di crescita epidermico N-terminale, un dominio legante la membrana di circa 48 aminoacidi di lunghezza che ancora la proteina a un lembo del doppio strato lipidico e un grande dominio catalitico globulare C-terminale con il sito attivo della cicloossigenasi che ospita il substrato o gli inibitori e quello della perossidasi che contiene il cofattore eme.
Il sito C-terminale contiene due siti attivi globulari distinti che richiedono substrati diversi ovvero il sito di perossidasi tasca dell’enzima che sporge verso l’esterno in cui vi sono gli amminoacidi His388 che coordina l’eme e Tyr385 che fa da tramite tra i due siti catalitici e il sito di cicloossigenasi.
Quest’ultimo è una stretta tasca a carattere idrofobico che si protrae interno all’enzima il cui imbocco è interno alle quattro α eliche costituenti il dominio di legame alla membrana e possiede un punto di costrizione formato da una rete di legami a idrogeno tra Tyr355, Arg120 e Glu524
Meccanismo di reazione
Il primo passo nella conversione dell’acido arachidonico nell’idroperossi-endoperossido, è l’estrazione dell’atomo di idrogeno dal carbonio-13. Il ciclo della perossidasi porta all’estrazione di un atomo di idrogeno dal Tyr-385 formando un radicale tirosilico e attivando il sito attivo della cicloossigenasi.
Il radicale tirosilico estrae l’atomo di idrogeno dal carbonio-13 dell’acido arachidonico, dando inizio alla reazione della cicloossigenasi, la cui fase finale rigenera il radicale tirosilico.
Lo stadio finale della reazione, la riduzione del radicale perossilico in idroperossido per formare prostaglandina 2, rigenera il radicale tirosilico. Pertanto, la cicloossigenasi attivata può effettuare più turnover senza la necessità di ripetere la fase di attivazione. Dopo aver avviato la reazione della ciclossigenasi, la funzione primaria della perossidasi è quella di ridurre il 15-idroperossi della prostaglandina 2 nel corrispondente alcol
Cicloossigenasi e farmaci antinfiammatori
L’uso di sostanze medicinali per la cura del dolore e della febbre risale alle antiche civiltà egizia e greca, dove erano usate foglie essiccate di mirto o estratti amari della corteccia di pioppo. Ippocrate prescriveva la corteccia e le foglie del salice per ridurre la febbre e alleviare il dolore del parto. Il componente attivo della corteccia di salice è stato successivamente identificato come salicina, che viene metabolizzata in salicilato.

Nel 1897, Felix Hoffmann della Bayer Company sviluppò una forma di salicilato sintetizzando l’acido acetilsalicilico, che fu chiamato “aspirina” e distribuito dalla Bayer sotto forma di compresse e polvere nel 1899.
Lo studio delle prostaglandine consentirono di individuare l’aspirina e altri farmaci antinfiammatori non steroidei come specie che inibiscono l’attività dell’enzima che converte gli acidi grassi polinsaturi in prostaglandine durante il processo infiammatorio. La cicloossigenasi catalizza la deossigenazione dell’acido arachidonico per formare la prostaglandina PGH2.
I principali effetti farmacologici dei FANS derivano pertanto dalla loro capacità di inibire le cicloossigenasi e le evidenze suggeriscono che le proprietà antinfiammatorie e analgesiche dei FANS tradizionali sono dovute all’inibizione della cocloosigenasi-2, mentre gli effetti collaterali di questi inibitori sono associati all’inibizione della cicloossigenasi-1. A causa della differenza nei profili di espressione tra la COX-1 e la COX-2, negli anni ’90 è stata avanzata l’ipotesi che gli inibitori selettivi della COX-2 condividessero le proprietà antinfiammatorie benefiche dei FANS tradizionali ma non presentassero la tossicità gastrica associata a questi composti.



