Geometria molecolare: la teoria V.S.E.P.R.
La geometria molecolare, ovvero il modo in cui gli atomi che costituiscono una molecola si dispongono nel piano o nello spazio, può essere prevista dalla teoria V.S.E.P.R. ( Valence Shell Electron Pair Repulsion) ovvero repulsione delle coppie elettroniche dello strato di valenza.
Secondo questa teoria, le coppie elettroniche disposte sull’ultimo livello dell’atomo centrale tendono a disporsi il più lontano possibile tra loro, per effetto della repulsione, il che dà origine a una precisa disposizione degli atomi nello spazio, quindi a una precisa geometria della molecola.
Principi
I principi fondamentali per ottenere la geometria molecolare sono i seguenti:
- Le coppie elettroniche interessate sono sia quelle impegnate nei legami che l’atomo centrale stabilisce con gli altri atomi (coppie condivise), sia quelle libere (coppie non condivise), purché appartenenti all’ultimo livello.
- I doppi e i tripli legami si considerano come un legame semplice, in quanto la nuvola elettronica del legame multiplo ha un’unica direzione e l’effetto è quindi lo stesso di un’unica coppia.
- Le coppie non condivise, essendo più dilatate nello spazio di quelle impegnate in un legame, esercitano una forza repulsiva più intensa sulle altre coppie, fattore che influisce sul valore dell’angolo di legame
La tabella di correlazione tra coppie elettroniche degli orbitali di valenza e la disposizione spaziale degli atomi in una molecola è la seguente:
| N. di coppie | Coppie di legame | Coppie non condivise | Geometria molecolare | Esempio |
| 2 | 2 | 0 | Lineare | BeCl2 |
| 3 | 3 | 0 | Triangolare | NO3– |
| 3 | 2 | 1 | Angolare | NO2– |
| 4 | 4 | 0 | Tetraedrica | CH4 |
| 4 | 3 | 1 | Piramidale trigonale | NH3 |
| 4 | 2 | 2 | Angolare | H2O |
| 5 | 4 | 1 | Tetraedrica distorta | TlCl4 |
| 5 | 3 | 2 | a T | ClF3 |
| 5 | 2 | 3 | Lineare | I3– |
| 6 | 6 | 0 | Ottaedrica | SF6 |
| 6 | 5 | 1 | Piramidale quadrata | IF5 |
| 6 | 4 | 2 | Quadrata | ICl4– |
| 5 | 5 | 0 | Bipiramidale trigonale | PCl5 |
Sulla base di tali regole generali, si possono dunque ottenere le disposizioni spaziali degli atomi in una molecola.
Esempi
Un esempio è costituito dal cloruro di berillio: il berillio, numero atomico = 4 ha configurazione elettronica 1s2, 2s2. A seguito della promozione di un elettrone dall’orbitale 2s a quello 2p il berillio presenta solo due elettroni spaiati e nessuna coppia elettronica non condivisa nel guscio di valenza e può essere rappresentata dalla struttura di Lewis

Attorno all’atomo di berillio centrale sono disposte due coppie di elettroni: esse si dovranno disporre, per rendere minima la repulsione, da parti opposte, per cui la struttura della molecola sarà lineare.
Come esempio di struttura con tra coppie di elettroni di legame e nessuna coppia non condivisa consideriamo lo ione nitrato che si presenta in tre forme limite di risonanza come da figura:
gli angoli di legame sono tutti di 120°.
Lo ione nitrito che si presenta in due forme di risonanza come da figura:
invece, presentando due coppie di legame e una coppia non condivisa, presenta un angolo di 115°C.

Nel caso di quattro coppie elettroniche condivise, come nel caso del metano , si ha una geometria tetraedrica con angoli di legame di 109.28°
Come esempio di tre coppie di legame e una non condivisa, si può citare l’ammoniaca la cui geometria è piramidale trigonale. Si può immaginare che la coppia elettronica non condivisa completi un tetraedro distorto come si può vedere in figura:

Un esempio di due coppie di legame condivise e due coppie non condivise è costituito dall’acqua in cui la distorsione del tetraedro è maggiore e infatti l’angolo di legame è di circa 104°
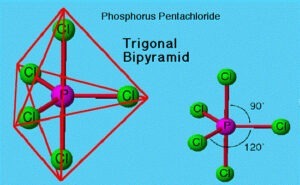
Nel caso di cinque coppie si hanno diverse possibilità: la disposizione più simmetrica è quella di cinque coppie di legame presenti, come ad esempio in pentacloruro di fosforo che avrà una geometria bipiramidale trigonale come da figura.
Mentre nel caso di quattro coppie condivise e
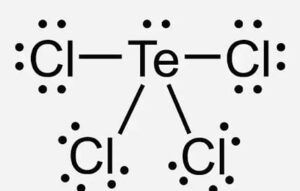
una non condivisa come per TeCl4 si avrà la geometria di un tetraedro distorto come si può vedere in figura
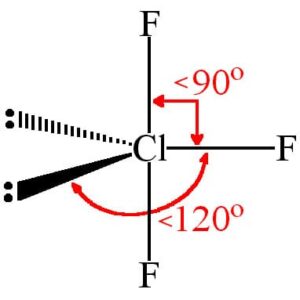
Due coppie non condivise e tre coppie di legame si hanno nella molecola ClF3 che ha una forma a T che è mostrata in figura.
Infine si può avere il caso di tre coppie non condivise e due condivise come nel caso dello ione triioduro I3– che mostra una struttura lineare

Resta infine il caso di sei coppie elettroniche: un esempio è costituito da SF6 che ha geometria ottaedrica:


La sostituzione di una coppia di legame con una non condivisa porta a una geometria piramidale quadrata come ad esempio in IF5
La sostituzione di due coppie di legame con due coppie non condivise porta, invece a una geometria planare quadrata come avviene ad esempio in ICl4–





